摘要:科學(xué)家們通過(guò)系統(tǒng)性的CRISPR篩選,發(fā)現(xiàn)PTGES3竟然是雄激素受體的一個(gè)意想不到的調(diào)節(jié)因子。
一種此前特性不明的蛋白質(zhì),過(guò)去被認(rèn)為是分子伴侶或酶,實(shí)際上可能在前列腺癌中扮演著關(guān)鍵角色。在一次系統(tǒng)的CRISPR篩選中,來(lái)自Arc研究所、加州大學(xué)舊金山分校和弗雷德·哈欽森癌癥中心的科學(xué)家們發(fā)現(xiàn),PTGES3(第三種前列腺素E合成酶)竟然是雄激素受體的一個(gè)意想不到的調(diào)節(jié)因子。這項(xiàng)發(fā)現(xiàn)于11月5日發(fā)表在《自然·遺傳學(xué)》雜志上,不僅重新定義了PTGES3在基因表達(dá)調(diào)控中的生物學(xué)作用,還揭示了一個(gè)有望用于治療對(duì)現(xiàn)有激素療法耐藥的侵襲性前列腺癌的新靶點(diǎn)。

圖1 全基因組CRISPR篩選鑒定PTGES3為晚期前列腺癌中雄激素受體的直接調(diào)節(jié)因子
研究團(tuán)隊(duì)在開(kāi)發(fā)出一種能夠?qū)崟r(shí)追蹤雄激素受體水平的熒光標(biāo)記后,發(fā)現(xiàn)了這種關(guān)聯(lián)。雄激素受體是一種激素感應(yīng)蛋白,通常有助于前列腺的發(fā)育和維持。在前列腺癌細(xì)胞中,雄激素受體活性顯著增強(qiáng),并驅(qū)動(dòng)腫瘤的侵襲性進(jìn)展,使其成為當(dāng)前治療的主要靶點(diǎn)。這項(xiàng)標(biāo)記技術(shù)的創(chuàng)新使得科學(xué)家能夠進(jìn)行全基因組CRISPR篩選,從而識(shí)別出哪些基因?qū)τ诰S持侵襲性前列腺癌細(xì)胞中的雄激素受體水平至關(guān)重要。
在篩選過(guò)程中,研究人員逐一關(guān)閉基因,以觀察哪些基因會(huì)導(dǎo)致發(fā)光的雄激素受體蛋白消失。篩選結(jié)果證實(shí)了已知的雄激素受體調(diào)節(jié)因子,例如 HOXB13 和 GATA2,驗(yàn)證了該方法的有效性,但也發(fā)現(xiàn)了一些意想不到的候選基因,例如 PTGES3。由于 PTGES3 是三種相關(guān)的合成前列腺素酶中唯一影響雄激素受體水平的酶,因此結(jié)果表明它可能并非之前認(rèn)為的那樣發(fā)揮作用。
“我們的研究展現(xiàn)了CRISPR技術(shù)在定量、無(wú)偏倚的蛋白質(zhì)研究中的強(qiáng)大作用,它能幫助我們發(fā)現(xiàn)一些關(guān)于研究充分的蛋白質(zhì)的新信息,”資深作者盧克·吉爾伯特(Luke Gilbert,@LukeGilbertSF)說(shuō)道,他是Arc研究所的核心研究員,也是加州大學(xué)舊金山分校醫(yī)學(xué)院泌尿外科副教授?!拔覀冏畛醯哪繕?biāo)是尋找可能調(diào)控雄激素受體生物學(xué)的酶,因?yàn)樗鼈兪撬幬锇悬c(diǎn),但最終我們發(fā)現(xiàn)了PTGES3,一種據(jù)我們所知并非酶的蛋白質(zhì),它卻對(duì)雄激素受體產(chǎn)生了深遠(yuǎn)的影響。”
為了進(jìn)一步探究PTGES3在前列腺癌中的潛在作用,研究團(tuán)隊(duì)分析了患者數(shù)據(jù),結(jié)果顯示PTGES3高表達(dá)的患者在接受激素治療后療效顯著較差。小鼠研究表明,抑制PTGES3可延緩腫瘤生長(zhǎng)并降低腫瘤內(nèi)雄激素受體水平,提示PTGES3可能成為治療耐藥性癌癥的新靶點(diǎn)。
研究人員證實(shí),在癌細(xì)胞中,PTGES3 實(shí)際上通過(guò)雙重機(jī)制發(fā)揮作用:一方面,它作為輔助伴侶蛋白,幫助穩(wěn)定細(xì)胞質(zhì)中的雄激素受體蛋白;另一方面,它作為核內(nèi)輔助因子,使雄激素受體能夠與 DNA 結(jié)合并激活其靶基因。如果雄激素受體是前列腺癌進(jìn)展的驅(qū)動(dòng)因素,那么研究人員提供的證據(jù)表明,腫瘤生長(zhǎng)可能受到 PTGES3 的輔助,甚至依賴于 PTGES3。
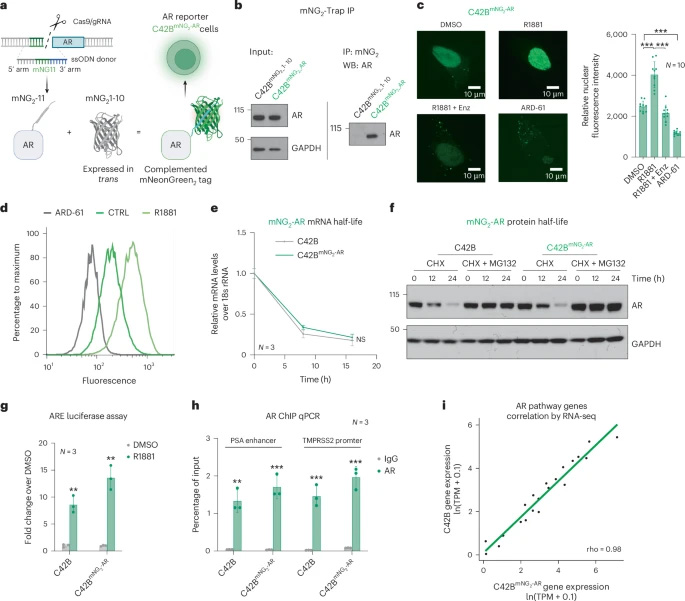
圖2 在PCa細(xì)胞中建立內(nèi)源性AR-mNG2熒光報(bào)告基因
“以往通過(guò)調(diào)控轉(zhuǎn)錄因子功能進(jìn)行治療的研究主要集中在DNA結(jié)合域和轉(zhuǎn)錄激活域。而針對(duì)轉(zhuǎn)錄因子穩(wěn)定性調(diào)控因子的研究則相對(duì)較少,”該研究的第一作者李浩龍(音譯)說(shuō)道。他曾在加州大學(xué)舊金山分校(UCSF)開(kāi)展這項(xiàng)研究,目前是弗雷德·哈欽森癌癥研究中心(Fred Hutch)的助理教授?!拔覀兊难芯靠梢詾槔斫獠煌に仳?qū)動(dòng)型癌癥中其他重要的轉(zhuǎn)錄因子提供參考模板。未來(lái),腫瘤學(xué)研究中至少有20種轉(zhuǎn)錄因子可以從這種方法中受益。”
研究團(tuán)隊(duì)目前正致力于了解PTGES3與雄激素受體相互作用的結(jié)構(gòu)細(xì)節(jié)。他們的長(zhǎng)期目標(biāo)是開(kāi)發(fā)針對(duì)這種相互作用的治療方法,可能采用已在臨床試驗(yàn)中展現(xiàn)出前景的蛋白質(zhì)降解策略。
該研究的另一位資深作者,加州大學(xué)舊金山分校海倫·迪勒家族綜合癌癥中心放射腫瘤學(xué)、泌尿外科和內(nèi)科學(xué)教授、轉(zhuǎn)化研究副主任Felix Feng于去年12月去世?!拔覀兩钋芯拺奄M(fèi)利克斯,并希望這項(xiàng)研究能成為他留下的寶貴遺產(chǎn),”吉爾伯特說(shuō)道。
參考資料
[1] Genome-scale CRISPR screens identify PTGES3 as a direct modulator of androgen receptor function in advanced prostate cancer
摘要:科學(xué)家們通過(guò)系統(tǒng)性的CRISPR篩選,發(fā)現(xiàn)PTGES3竟然是雄激素受體的一個(gè)意想不到的調(diào)節(jié)因子。
一種此前特性不明的蛋白質(zhì),過(guò)去被認(rèn)為是分子伴侶或酶,實(shí)際上可能在前列腺癌中扮演著關(guān)鍵角色。在一次系統(tǒng)的CRISPR篩選中,來(lái)自Arc研究所、加州大學(xué)舊金山分校和弗雷德·哈欽森癌癥中心的科學(xué)家們發(fā)現(xiàn),PTGES3(第三種前列腺素E合成酶)竟然是雄激素受體的一個(gè)意想不到的調(diào)節(jié)因子。這項(xiàng)發(fā)現(xiàn)于11月5日發(fā)表在《自然·遺傳學(xué)》雜志上,不僅重新定義了PTGES3在基因表達(dá)調(diào)控中的生物學(xué)作用,還揭示了一個(gè)有望用于治療對(duì)現(xiàn)有激素療法耐藥的侵襲性前列腺癌的新靶點(diǎn)。

圖1 全基因組CRISPR篩選鑒定PTGES3為晚期前列腺癌中雄激素受體的直接調(diào)節(jié)因子
研究團(tuán)隊(duì)在開(kāi)發(fā)出一種能夠?qū)崟r(shí)追蹤雄激素受體水平的熒光標(biāo)記后,發(fā)現(xiàn)了這種關(guān)聯(lián)。雄激素受體是一種激素感應(yīng)蛋白,通常有助于前列腺的發(fā)育和維持。在前列腺癌細(xì)胞中,雄激素受體活性顯著增強(qiáng),并驅(qū)動(dòng)腫瘤的侵襲性進(jìn)展,使其成為當(dāng)前治療的主要靶點(diǎn)。這項(xiàng)標(biāo)記技術(shù)的創(chuàng)新使得科學(xué)家能夠進(jìn)行全基因組CRISPR篩選,從而識(shí)別出哪些基因?qū)τ诰S持侵襲性前列腺癌細(xì)胞中的雄激素受體水平至關(guān)重要。
在篩選過(guò)程中,研究人員逐一關(guān)閉基因,以觀察哪些基因會(huì)導(dǎo)致發(fā)光的雄激素受體蛋白消失。篩選結(jié)果證實(shí)了已知的雄激素受體調(diào)節(jié)因子,例如 HOXB13 和 GATA2,驗(yàn)證了該方法的有效性,但也發(fā)現(xiàn)了一些意想不到的候選基因,例如 PTGES3。由于 PTGES3 是三種相關(guān)的合成前列腺素酶中唯一影響雄激素受體水平的酶,因此結(jié)果表明它可能并非之前認(rèn)為的那樣發(fā)揮作用。
“我們的研究展現(xiàn)了CRISPR技術(shù)在定量、無(wú)偏倚的蛋白質(zhì)研究中的強(qiáng)大作用,它能幫助我們發(fā)現(xiàn)一些關(guān)于研究充分的蛋白質(zhì)的新信息,”資深作者盧克·吉爾伯特(Luke Gilbert,@LukeGilbertSF)說(shuō)道,他是Arc研究所的核心研究員,也是加州大學(xué)舊金山分校醫(yī)學(xué)院泌尿外科副教授。“我們最初的目標(biāo)是尋找可能調(diào)控雄激素受體生物學(xué)的酶,因?yàn)樗鼈兪撬幬锇悬c(diǎn),但最終我們發(fā)現(xiàn)了PTGES3,一種據(jù)我們所知并非酶的蛋白質(zhì),它卻對(duì)雄激素受體產(chǎn)生了深遠(yuǎn)的影響。”
為了進(jìn)一步探究PTGES3在前列腺癌中的潛在作用,研究團(tuán)隊(duì)分析了患者數(shù)據(jù),結(jié)果顯示PTGES3高表達(dá)的患者在接受激素治療后療效顯著較差。小鼠研究表明,抑制PTGES3可延緩腫瘤生長(zhǎng)并降低腫瘤內(nèi)雄激素受體水平,提示PTGES3可能成為治療耐藥性癌癥的新靶點(diǎn)。
研究人員證實(shí),在癌細(xì)胞中,PTGES3 實(shí)際上通過(guò)雙重機(jī)制發(fā)揮作用:一方面,它作為輔助伴侶蛋白,幫助穩(wěn)定細(xì)胞質(zhì)中的雄激素受體蛋白;另一方面,它作為核內(nèi)輔助因子,使雄激素受體能夠與 DNA 結(jié)合并激活其靶基因。如果雄激素受體是前列腺癌進(jìn)展的驅(qū)動(dòng)因素,那么研究人員提供的證據(jù)表明,腫瘤生長(zhǎng)可能受到 PTGES3 的輔助,甚至依賴于 PTGES3。

圖2 在PCa細(xì)胞中建立內(nèi)源性AR-mNG2熒光報(bào)告基因
“以往通過(guò)調(diào)控轉(zhuǎn)錄因子功能進(jìn)行治療的研究主要集中在DNA結(jié)合域和轉(zhuǎn)錄激活域。而針對(duì)轉(zhuǎn)錄因子穩(wěn)定性調(diào)控因子的研究則相對(duì)較少,”該研究的第一作者李浩龍(音譯)說(shuō)道。他曾在加州大學(xué)舊金山分校(UCSF)開(kāi)展這項(xiàng)研究,目前是弗雷德·哈欽森癌癥研究中心(Fred Hutch)的助理教授?!拔覀兊难芯靠梢詾槔斫獠煌に仳?qū)動(dòng)型癌癥中其他重要的轉(zhuǎn)錄因子提供參考模板。未來(lái),腫瘤學(xué)研究中至少有20種轉(zhuǎn)錄因子可以從這種方法中受益?!?/div>
研究團(tuán)隊(duì)目前正致力于了解PTGES3與雄激素受體相互作用的結(jié)構(gòu)細(xì)節(jié)。他們的長(zhǎng)期目標(biāo)是開(kāi)發(fā)針對(duì)這種相互作用的治療方法,可能采用已在臨床試驗(yàn)中展現(xiàn)出前景的蛋白質(zhì)降解策略。
該研究的另一位資深作者,加州大學(xué)舊金山分校海倫·迪勒家族綜合癌癥中心放射腫瘤學(xué)、泌尿外科和內(nèi)科學(xué)教授、轉(zhuǎn)化研究副主任Felix Feng于去年12月去世。“我們深切緬懷費(fèi)利克斯,并希望這項(xiàng)研究能成為他留下的寶貴遺產(chǎn),”吉爾伯特說(shuō)道。
參考資料
[1] Genome-scale CRISPR screens identify PTGES3 as a direct modulator of androgen receptor function in advanced prostate cancer



