摘要: 本綜述深入探討了免疫代謝在腫瘤微環(huán)境(TME)中的關(guān)鍵作用。
免疫細(xì)胞代謝在調(diào)節(jié)細(xì)胞增殖、分化和功能反應(yīng)中發(fā)揮著關(guān)鍵作用,共同塑造著腫瘤微環(huán)境(TME)內(nèi)的免疫應(yīng)答。 近期的研究進(jìn)展日益凸顯了免疫細(xì)胞多樣化的代謝表型及其與腫瘤動態(tài)之間復(fù)雜的相互作用。免疫細(xì)胞代謝展現(xiàn)出顯著的可塑性,使得代謝網(wǎng)絡(luò)能夠根據(jù)外部刺激精確地調(diào)控免疫細(xì)胞的行為。此外,在免疫代謝學(xué)研究中,代謝特征與免疫細(xì)胞命運、活化狀態(tài)及功能之間的強關(guān)聯(lián)性已被反復(fù)闡明。因此,靶向被稱為“代謝檢查點”的代謝網(wǎng)絡(luò),以重編程免疫細(xì)胞表型并增強抗腫瘤免疫力,為臨床轉(zhuǎn)化帶來了重大希望。本綜述總結(jié)了多層面代謝檢查點的最新研究進(jìn)展,重點探討了代謝檢查點如何調(diào)控免疫學(xué)效應(yīng)及癌癥進(jìn)展。最后,文章探討了靶向代謝檢查點的潛在策略,以期為免疫治療領(lǐng)域啟發(fā)創(chuàng)新方法。
免疫代謝與腫瘤微環(huán)境的博弈
免疫細(xì)胞代謝在腫瘤微環(huán)境(TME)中扮演著決定性角色。不同于傳統(tǒng)觀點將代謝視為能量供應(yīng)的被動過程,最新研究揭示代謝網(wǎng)絡(luò)主動調(diào)控著免疫細(xì)胞的增殖、分化和功能應(yīng)答。這種代謝可塑性為癌癥免疫治療提供了全新靶點。

圖1 免疫細(xì)胞重塑中的代謝檢查點:重編程免疫代謝用于癌癥治療
代謝壓力下的腫瘤戰(zhàn)場
TME是一個營養(yǎng)匱乏、缺氧、酸性的惡劣環(huán)境。癌細(xì)胞通過Warburg效應(yīng)大量消耗葡萄糖,產(chǎn)生乳酸堆積,同時競爭性攝取氨基酸如甲硫氨酸和精氨酸。這種代謝壓力直接抑制了CD8+ T細(xì)胞的mTOR活性和IFN-γ產(chǎn)生。有趣的是,乳酸雖能抑制常規(guī)DC細(xì)胞和NK細(xì)胞功能,卻意外地增強了CD8+ T細(xì)胞的干性特征。
T細(xì)胞的代謝交響曲
初始T細(xì)胞主要依賴氧化磷酸化(OXPHOS)維持靜息狀態(tài),而激活后的效應(yīng)T細(xì)胞則轉(zhuǎn)向有氧糖酵解以滿足快速增殖需求。這一轉(zhuǎn)換受mTORC1/2復(fù)合物調(diào)控,并通過MYC和HIF-1α上調(diào)GLUT1和HK2表達(dá)。值得注意的是,GLUT1在Th1、Th2和Th17細(xì)胞分化中不可或缺,但對Treg細(xì)胞卻非必需。
氨基酸代謝的暗戰(zhàn)
癌細(xì)胞通過高表達(dá)SLC43A2轉(zhuǎn)運體與T細(xì)胞競爭甲硫氨酸,降低組蛋白H3K4甲基化水平,從而抑制Th17細(xì)胞功能。精氨酸代謝同樣關(guān)鍵,腫瘤相關(guān)MDSC高表達(dá)精氨酸酶1(Arg1),消耗微環(huán)境中的精氨酸,導(dǎo)致T細(xì)胞CD3ζ鏈表達(dá)下降和功能衰竭。而靶向SLC7A11介導(dǎo)的胱氨酸代謝可防止CD8+ T細(xì)胞鐵死亡,增強抗腫瘤免疫。
脂質(zhì)代謝的雙刃劍
CD36介導(dǎo)的氧化脂質(zhì)攝取會誘發(fā)CD8+ T細(xì)胞鐵死亡和衰竭,但卻是Treg細(xì)胞維持免疫抑制功能所必需的。膽固醇代謝同樣具有兩面性:ACAT1缺失可增加T細(xì)胞膜膽固醇水平,增強免疫突觸形成;但過量膽固醇又會引發(fā)內(nèi)質(zhì)網(wǎng)應(yīng)激,促進(jìn)T細(xì)胞耗竭。
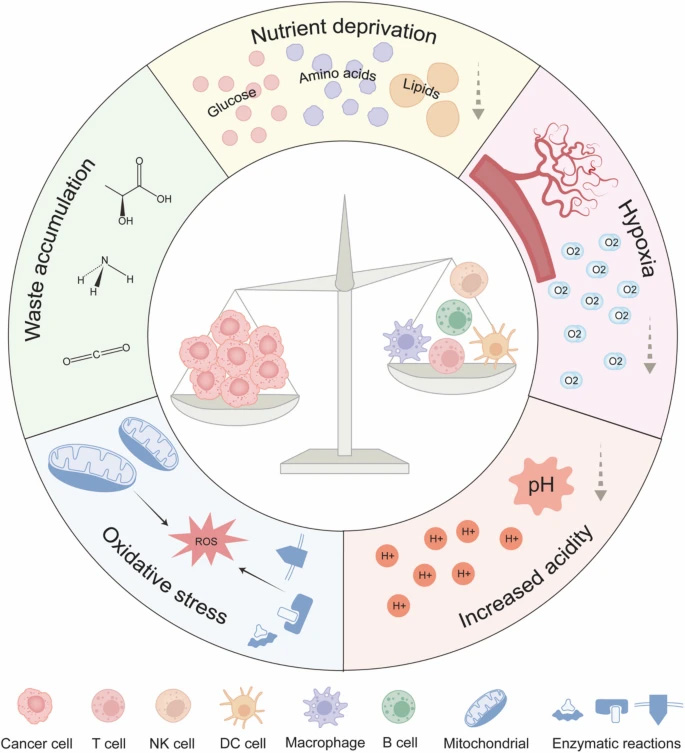
圖2 腫瘤微環(huán)境中的代謝壓力
代謝干預(yù)的治療曙光
臨床前研究展示了多種有前景的策略:JHU083通過抑制谷氨酰胺代謝同時增強T細(xì)胞OXPHOS;乳酸氧化酶納米膠囊降低TME酸度;精氨酸補充劑與化療聯(lián)用可重塑記憶T細(xì)胞代謝。值得注意的是,IDO/TDO雙重抑制劑較單藥顯示出更好的協(xié)同效應(yīng),而CRISPR技術(shù)敲除LDHA可改善TME免疫狀態(tài)。
未來挑戰(zhàn)與展望
盡管前景廣闊,代謝治療仍面臨重大挑戰(zhàn):不同免疫細(xì)胞代謝網(wǎng)絡(luò)相互交織;代謝物如乳酸的雙向作用;以及如何實現(xiàn)時空特異性干預(yù)。整合單細(xì)胞代謝組學(xué)、微生物組調(diào)控等新技術(shù)將有助于突破當(dāng)前局限,開創(chuàng)癌癥免疫治療新紀(jì)元。
參考資料
[1] Metabolic checkpoints in immune cell reprogramming: rewiring immunometabolism for cancer therapy
摘要: 本綜述深入探討了免疫代謝在腫瘤微環(huán)境(TME)中的關(guān)鍵作用。
免疫細(xì)胞代謝在調(diào)節(jié)細(xì)胞增殖、分化和功能反應(yīng)中發(fā)揮著關(guān)鍵作用,共同塑造著腫瘤微環(huán)境(TME)內(nèi)的免疫應(yīng)答。 近期的研究進(jìn)展日益凸顯了免疫細(xì)胞多樣化的代謝表型及其與腫瘤動態(tài)之間復(fù)雜的相互作用。免疫細(xì)胞代謝展現(xiàn)出顯著的可塑性,使得代謝網(wǎng)絡(luò)能夠根據(jù)外部刺激精確地調(diào)控免疫細(xì)胞的行為。此外,在免疫代謝學(xué)研究中,代謝特征與免疫細(xì)胞命運、活化狀態(tài)及功能之間的強關(guān)聯(lián)性已被反復(fù)闡明。因此,靶向被稱為“代謝檢查點”的代謝網(wǎng)絡(luò),以重編程免疫細(xì)胞表型并增強抗腫瘤免疫力,為臨床轉(zhuǎn)化帶來了重大希望。本綜述總結(jié)了多層面代謝檢查點的最新研究進(jìn)展,重點探討了代謝檢查點如何調(diào)控免疫學(xué)效應(yīng)及癌癥進(jìn)展。最后,文章探討了靶向代謝檢查點的潛在策略,以期為免疫治療領(lǐng)域啟發(fā)創(chuàng)新方法。
免疫代謝與腫瘤微環(huán)境的博弈
免疫細(xì)胞代謝在腫瘤微環(huán)境(TME)中扮演著決定性角色。不同于傳統(tǒng)觀點將代謝視為能量供應(yīng)的被動過程,最新研究揭示代謝網(wǎng)絡(luò)主動調(diào)控著免疫細(xì)胞的增殖、分化和功能應(yīng)答。這種代謝可塑性為癌癥免疫治療提供了全新靶點。

圖1 免疫細(xì)胞重塑中的代謝檢查點:重編程免疫代謝用于癌癥治療
代謝壓力下的腫瘤戰(zhàn)場
TME是一個營養(yǎng)匱乏、缺氧、酸性的惡劣環(huán)境。癌細(xì)胞通過Warburg效應(yīng)大量消耗葡萄糖,產(chǎn)生乳酸堆積,同時競爭性攝取氨基酸如甲硫氨酸和精氨酸。這種代謝壓力直接抑制了CD8+ T細(xì)胞的mTOR活性和IFN-γ產(chǎn)生。有趣的是,乳酸雖能抑制常規(guī)DC細(xì)胞和NK細(xì)胞功能,卻意外地增強了CD8+ T細(xì)胞的干性特征。
T細(xì)胞的代謝交響曲
初始T細(xì)胞主要依賴氧化磷酸化(OXPHOS)維持靜息狀態(tài),而激活后的效應(yīng)T細(xì)胞則轉(zhuǎn)向有氧糖酵解以滿足快速增殖需求。這一轉(zhuǎn)換受mTORC1/2復(fù)合物調(diào)控,并通過MYC和HIF-1α上調(diào)GLUT1和HK2表達(dá)。值得注意的是,GLUT1在Th1、Th2和Th17細(xì)胞分化中不可或缺,但對Treg細(xì)胞卻非必需。
氨基酸代謝的暗戰(zhàn)
癌細(xì)胞通過高表達(dá)SLC43A2轉(zhuǎn)運體與T細(xì)胞競爭甲硫氨酸,降低組蛋白H3K4甲基化水平,從而抑制Th17細(xì)胞功能。精氨酸代謝同樣關(guān)鍵,腫瘤相關(guān)MDSC高表達(dá)精氨酸酶1(Arg1),消耗微環(huán)境中的精氨酸,導(dǎo)致T細(xì)胞CD3ζ鏈表達(dá)下降和功能衰竭。而靶向SLC7A11介導(dǎo)的胱氨酸代謝可防止CD8+ T細(xì)胞鐵死亡,增強抗腫瘤免疫。
脂質(zhì)代謝的雙刃劍
CD36介導(dǎo)的氧化脂質(zhì)攝取會誘發(fā)CD8+ T細(xì)胞鐵死亡和衰竭,但卻是Treg細(xì)胞維持免疫抑制功能所必需的。膽固醇代謝同樣具有兩面性:ACAT1缺失可增加T細(xì)胞膜膽固醇水平,增強免疫突觸形成;但過量膽固醇又會引發(fā)內(nèi)質(zhì)網(wǎng)應(yīng)激,促進(jìn)T細(xì)胞耗竭。

圖2 腫瘤微環(huán)境中的代謝壓力
代謝干預(yù)的治療曙光
臨床前研究展示了多種有前景的策略:JHU083通過抑制谷氨酰胺代謝同時增強T細(xì)胞OXPHOS;乳酸氧化酶納米膠囊降低TME酸度;精氨酸補充劑與化療聯(lián)用可重塑記憶T細(xì)胞代謝。值得注意的是,IDO/TDO雙重抑制劑較單藥顯示出更好的協(xié)同效應(yīng),而CRISPR技術(shù)敲除LDHA可改善TME免疫狀態(tài)。
未來挑戰(zhàn)與展望
盡管前景廣闊,代謝治療仍面臨重大挑戰(zhàn):不同免疫細(xì)胞代謝網(wǎng)絡(luò)相互交織;代謝物如乳酸的雙向作用;以及如何實現(xiàn)時空特異性干預(yù)。整合單細(xì)胞代謝組學(xué)、微生物組調(diào)控等新技術(shù)將有助于突破當(dāng)前局限,開創(chuàng)癌癥免疫治療新紀(jì)元。
參考資料
[1] Metabolic checkpoints in immune cell reprogramming: rewiring immunometabolism for cancer therapy



