摘要:研究通過單核RNA測序技術(shù)構(gòu)建了P8小鼠海馬細(xì)胞圖譜,開發(fā)了機器學(xué)習(xí)分類器精準(zhǔn)識別細(xì)胞類型。
新生兒缺氧缺血性腦損傷是導(dǎo)致嬰幼兒死亡和神經(jīng)發(fā)育障礙的首要原因,其中代謝活躍的海馬區(qū)尤為脆弱。目前臨床治療面臨兩大困境:一是缺乏針對早期損傷窗口的有效干預(yù)措施,二是對細(xì)胞類型特異性損傷機制認(rèn)識不足。傳統(tǒng)研究多聚焦于損傷后數(shù)天至數(shù)周的遲發(fā)性神經(jīng)元死亡,而決定損傷轉(zhuǎn)歸的關(guān)鍵早期事件仍如"黑箱"。
 圖1 早期轉(zhuǎn)錄應(yīng)答揭示新生兒缺血性海馬中細(xì)胞類型特異性的脆弱性與神經(jīng)保護(hù)機制
圖1 早期轉(zhuǎn)錄應(yīng)答揭示新生兒缺血性海馬中細(xì)胞類型特異性的脆弱性與神經(jīng)保護(hù)機制挪威科技大學(xué)等機構(gòu)的研究團隊在《Acta Neuropathologica Communications》發(fā)表突破性研究。研究人員采用改良Vannucci法建立P8(相當(dāng)于人類妊娠32-42周)小鼠缺氧缺血模型,通過單核RNA測序(snRNA-seq)結(jié)合獨創(chuàng)的機器學(xué)習(xí)分類系統(tǒng),繪制了包含42萬細(xì)胞的參考圖譜。研究創(chuàng)新性地開發(fā)了貝葉斯優(yōu)化算法驅(qū)動的細(xì)胞分類器,準(zhǔn)確率較傳統(tǒng)方法顯著提升。實驗設(shè)計包含假手術(shù)組、單純?nèi)毖踅M和缺氧缺血組,在損傷后3小時即開展分析,捕捉到常規(guī)方法難以檢測的早期轉(zhuǎn)錄事件。
關(guān)鍵技術(shù)包括:1)改良Vannucci法建立新生兒缺氧缺血模型;2)split-pool組合條形碼技術(shù)進(jìn)行單核轉(zhuǎn)錄組測序;3)整合33種細(xì)胞類型的海馬參考圖譜構(gòu)建;4)基于高斯過程優(yōu)化的機器學(xué)習(xí)分類算法開發(fā);5)SCENIC基因調(diào)控網(wǎng)絡(luò)分析;6)免疫熒光共聚焦驗證關(guān)鍵蛋白表達(dá)。
細(xì)胞特異性脆弱模式
通過機器學(xué)習(xí)輔助的細(xì)胞聚類,研究首次發(fā)現(xiàn)CA1區(qū)成熟神經(jīng)元在缺氧缺血3小時后即減少65.88%,而DG區(qū)未成熟顆粒細(xì)胞保持穩(wěn)定。免疫組化證實NeuNhigh成熟神經(jīng)元顯著減少,TUNEL檢測顯示DG顆粒細(xì)胞層凋亡增加。轉(zhuǎn)錄組分析揭示脆弱神經(jīng)元中核糖體生物合成通路異常激活,可能加劇能量危機。
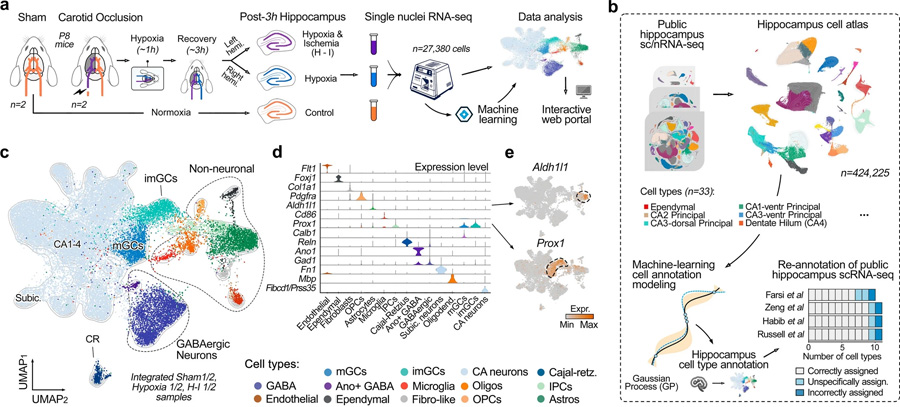
圖2 通過機器學(xué)習(xí)生成用于精確細(xì)胞類型注釋的綜合海馬圖譜
關(guān)鍵調(diào)控網(wǎng)絡(luò)解析
SCENIC分析鑒定出Hivep2、Bcl11a、Bcl6和Thra等轉(zhuǎn)錄因子構(gòu)成核心調(diào)控模塊,這些因子在脆弱神經(jīng)元中活性降低,導(dǎo)致鈣穩(wěn)態(tài)相關(guān)基因(如Cacnb2、Camk2a等)表達(dá)紊亂。有趣的是,抗壓神經(jīng)元中Klf12和Pdlim5調(diào)控網(wǎng)絡(luò)保持穩(wěn)定,Cajal-Retzius細(xì)胞通過激活Smoothened信號通路獲得保護(hù)。
膠質(zhì)細(xì)胞快速響應(yīng)
選擇性剔除實驗顯示,KCs而非樹突狀細(xì)胞(DCs)是CD4+ T細(xì)胞發(fā)揮作用的關(guān)鍵平臺。被"許可"(licensed)的KCs高表達(dá)MHC II和共刺激分子(CD40、CD80、CD86),并分泌IL-27。
IL-27的治療潛力
損傷3小時后即觀察到CD86+小膠質(zhì)細(xì)胞和GFAP+星形膠質(zhì)細(xì)胞比例增加。Runx1被鑒定為小膠質(zhì)細(xì)胞早期免疫反應(yīng)的關(guān)鍵調(diào)控因子,其靶基因涵蓋Ccl4、Il1a等炎癥因子和C1qb等吞噬相關(guān)基因。內(nèi)皮細(xì)胞則通過下調(diào)Tead4/Lef1發(fā)育程序,同時激活VEGFA和ANGPT2信號啟動血管修復(fù)。
這項研究開創(chuàng)性地繪制了新生兒腦損傷的早期分子圖譜,揭示了決定細(xì)胞命運的關(guān)鍵時間窗口。發(fā)現(xiàn)的Hivep2-Bcl11a調(diào)控模塊和Runx1靶向網(wǎng)絡(luò)為開發(fā)神經(jīng)保護(hù)藥物提供了新靶點。建立的hippo-seq.org平臺將成為領(lǐng)域重要資源,其機器學(xué)習(xí)分類算法成功糾正了既往研究中5種細(xì)胞的錯誤注釋。研究提出的"核糖體生物合成亢進(jìn)加劇神經(jīng)元損傷"新機制,為臨床聯(lián)合干預(yù)能量代謝和鈣穩(wěn)態(tài)紊亂提供了理論依據(jù)。該成果對改善新生兒腦損傷預(yù)后具有重要轉(zhuǎn)化價值,也為其他腦缺血疾病的治療策略開發(fā)提供了新思路。
參考資料
[1] Early transcriptional responses reveal cell type-specific vulnerability and neuroprotective mechanisms in the neonatal ischemic hippocampus
摘要:研究通過單核RNA測序技術(shù)構(gòu)建了P8小鼠海馬細(xì)胞圖譜,開發(fā)了機器學(xué)習(xí)分類器精準(zhǔn)識別細(xì)胞類型。
新生兒缺氧缺血性腦損傷是導(dǎo)致嬰幼兒死亡和神經(jīng)發(fā)育障礙的首要原因,其中代謝活躍的海馬區(qū)尤為脆弱。目前臨床治療面臨兩大困境:一是缺乏針對早期損傷窗口的有效干預(yù)措施,二是對細(xì)胞類型特異性損傷機制認(rèn)識不足。傳統(tǒng)研究多聚焦于損傷后數(shù)天至數(shù)周的遲發(fā)性神經(jīng)元死亡,而決定損傷轉(zhuǎn)歸的關(guān)鍵早期事件仍如"黑箱"。
 圖1 早期轉(zhuǎn)錄應(yīng)答揭示新生兒缺血性海馬中細(xì)胞類型特異性的脆弱性與神經(jīng)保護(hù)機制
圖1 早期轉(zhuǎn)錄應(yīng)答揭示新生兒缺血性海馬中細(xì)胞類型特異性的脆弱性與神經(jīng)保護(hù)機制挪威科技大學(xué)等機構(gòu)的研究團隊在《Acta Neuropathologica Communications》發(fā)表突破性研究。研究人員采用改良Vannucci法建立P8(相當(dāng)于人類妊娠32-42周)小鼠缺氧缺血模型,通過單核RNA測序(snRNA-seq)結(jié)合獨創(chuàng)的機器學(xué)習(xí)分類系統(tǒng),繪制了包含42萬細(xì)胞的參考圖譜。研究創(chuàng)新性地開發(fā)了貝葉斯優(yōu)化算法驅(qū)動的細(xì)胞分類器,準(zhǔn)確率較傳統(tǒng)方法顯著提升。實驗設(shè)計包含假手術(shù)組、單純?nèi)毖踅M和缺氧缺血組,在損傷后3小時即開展分析,捕捉到常規(guī)方法難以檢測的早期轉(zhuǎn)錄事件。
關(guān)鍵技術(shù)包括:1)改良Vannucci法建立新生兒缺氧缺血模型;2)split-pool組合條形碼技術(shù)進(jìn)行單核轉(zhuǎn)錄組測序;3)整合33種細(xì)胞類型的海馬參考圖譜構(gòu)建;4)基于高斯過程優(yōu)化的機器學(xué)習(xí)分類算法開發(fā);5)SCENIC基因調(diào)控網(wǎng)絡(luò)分析;6)免疫熒光共聚焦驗證關(guān)鍵蛋白表達(dá)。
細(xì)胞特異性脆弱模式
通過機器學(xué)習(xí)輔助的細(xì)胞聚類,研究首次發(fā)現(xiàn)CA1區(qū)成熟神經(jīng)元在缺氧缺血3小時后即減少65.88%,而DG區(qū)未成熟顆粒細(xì)胞保持穩(wěn)定。免疫組化證實NeuNhigh成熟神經(jīng)元顯著減少,TUNEL檢測顯示DG顆粒細(xì)胞層凋亡增加。轉(zhuǎn)錄組分析揭示脆弱神經(jīng)元中核糖體生物合成通路異常激活,可能加劇能量危機。

圖2 通過機器學(xué)習(xí)生成用于精確細(xì)胞類型注釋的綜合海馬圖譜
關(guān)鍵調(diào)控網(wǎng)絡(luò)解析
SCENIC分析鑒定出Hivep2、Bcl11a、Bcl6和Thra等轉(zhuǎn)錄因子構(gòu)成核心調(diào)控模塊,這些因子在脆弱神經(jīng)元中活性降低,導(dǎo)致鈣穩(wěn)態(tài)相關(guān)基因(如Cacnb2、Camk2a等)表達(dá)紊亂。有趣的是,抗壓神經(jīng)元中Klf12和Pdlim5調(diào)控網(wǎng)絡(luò)保持穩(wěn)定,Cajal-Retzius細(xì)胞通過激活Smoothened信號通路獲得保護(hù)。
膠質(zhì)細(xì)胞快速響應(yīng)
選擇性剔除實驗顯示,KCs而非樹突狀細(xì)胞(DCs)是CD4+ T細(xì)胞發(fā)揮作用的關(guān)鍵平臺。被"許可"(licensed)的KCs高表達(dá)MHC II和共刺激分子(CD40、CD80、CD86),并分泌IL-27。
IL-27的治療潛力
損傷3小時后即觀察到CD86+小膠質(zhì)細(xì)胞和GFAP+星形膠質(zhì)細(xì)胞比例增加。Runx1被鑒定為小膠質(zhì)細(xì)胞早期免疫反應(yīng)的關(guān)鍵調(diào)控因子,其靶基因涵蓋Ccl4、Il1a等炎癥因子和C1qb等吞噬相關(guān)基因。內(nèi)皮細(xì)胞則通過下調(diào)Tead4/Lef1發(fā)育程序,同時激活VEGFA和ANGPT2信號啟動血管修復(fù)。
這項研究開創(chuàng)性地繪制了新生兒腦損傷的早期分子圖譜,揭示了決定細(xì)胞命運的關(guān)鍵時間窗口。發(fā)現(xiàn)的Hivep2-Bcl11a調(diào)控模塊和Runx1靶向網(wǎng)絡(luò)為開發(fā)神經(jīng)保護(hù)藥物提供了新靶點。建立的hippo-seq.org平臺將成為領(lǐng)域重要資源,其機器學(xué)習(xí)分類算法成功糾正了既往研究中5種細(xì)胞的錯誤注釋。研究提出的"核糖體生物合成亢進(jìn)加劇神經(jīng)元損傷"新機制,為臨床聯(lián)合干預(yù)能量代謝和鈣穩(wěn)態(tài)紊亂提供了理論依據(jù)。該成果對改善新生兒腦損傷預(yù)后具有重要轉(zhuǎn)化價值,也為其他腦缺血疾病的治療策略開發(fā)提供了新思路。
參考資料
[1] Early transcriptional responses reveal cell type-specific vulnerability and neuroprotective mechanisms in the neonatal ischemic hippocampus



