摘要:一種以前未被發(fā)現(xiàn)的蛋白質(zhì)的功能,在細(xì)胞應(yīng)激過程中對(duì)RNA修復(fù)很重要。。
核糖核酸(rna)是單鏈分子,在所有生物體的細(xì)胞中起著至關(guān)重要的作用。例如,作為我們基因的“轉(zhuǎn)錄本”,mRNA通過自己的序列攜帶制造蛋白質(zhì)的指令,參與了遺傳信息的翻譯??邓固勾拇髮W(xué)(University of Konstanz)有機(jī)和細(xì)胞化學(xué)教授Andreas Marx解釋說:“為了在細(xì)胞中發(fā)揮不同的功能,RNA通常需要進(jìn)行化學(xué)修飾,或在受損后進(jìn)行修復(fù)?!?/div>
圖1 蛋白質(zhì)C12orf29具有抵抗細(xì)胞應(yīng)激的保護(hù)功能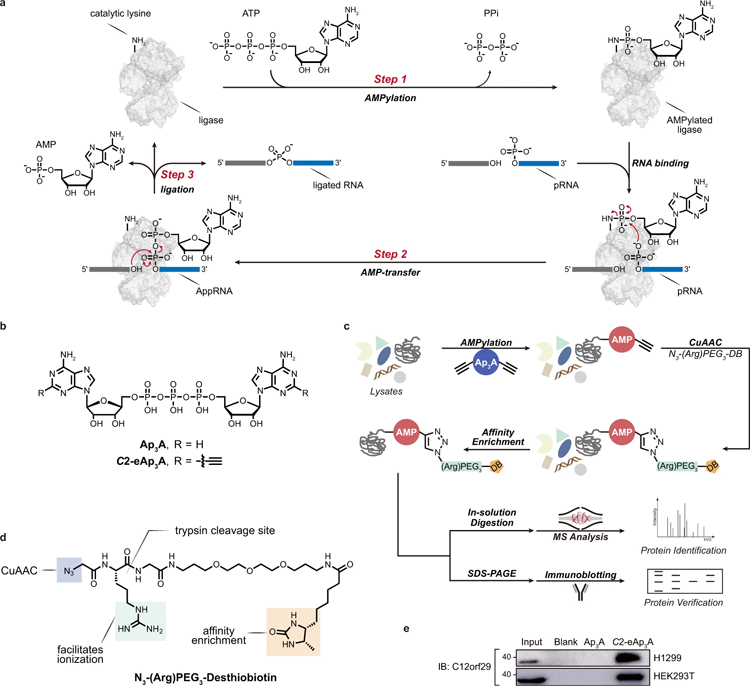
圖2 RNA連接酶機(jī)制和用修飾的Ap3A探針通過化學(xué)蛋白質(zhì)組學(xué)鑒定C12orf29
其中起作用的一種化學(xué)反應(yīng)是兩條RNA鏈在各自的兩端進(jìn)行三步連接(結(jié)扎)。這種反應(yīng)是由一種叫做RNA連接酶的特殊酶引發(fā)的,從病毒到真菌和植物,這種反應(yīng)存在于所有形式的生命中。在包括人類在內(nèi)的脊椎動(dòng)物中,這種RNA連接酶尚未被發(fā)現(xiàn)。來自康斯坦茨的一個(gè)跨學(xué)科研究小組現(xiàn)在發(fā)現(xiàn)了這種類型的第一個(gè)人類RNA連接酶:蛋白質(zhì)C12orf29。在細(xì)胞水平上,發(fā)表在《自然通訊》上的研究結(jié)果表明,這種酶具有抵抗細(xì)胞應(yīng)激的保護(hù)功能。

圖1 蛋白質(zhì)C12orf29具有抵抗細(xì)胞應(yīng)激的保護(hù)功能
“我們?cè)趯?duì)人類肺癌和腎細(xì)胞的廣泛研究中注意到C12orf29,我們?cè)趯ふ揖哂刑囟ɑ瘜W(xué)特征的蛋白質(zhì)時(shí)使用了新的化學(xué)工具。它引起了我們的注意,因?yàn)樵谀侵?,人們還不知道這種蛋白質(zhì)的功能是什么,”因此,研究人員開發(fā)并使用了各種方案來純化和預(yù)測(cè)未開發(fā)蛋白質(zhì)的結(jié)構(gòu),并進(jìn)行實(shí)驗(yàn)來追蹤其化學(xué)功能。因此,他們能夠證明最初只是一個(gè)合理的懷疑:C12orf29使用三磷酸腺苷(ATP)連接RNA鏈。
研究人員能夠詳細(xì)地展示這個(gè)過程遵循一個(gè)特征,從其他生命形式的其他RNA連接酶中已知的三步反應(yīng)模式。為了進(jìn)一步了解C12orf29在細(xì)胞水平上的功能,研究人員在闡明了化學(xué)機(jī)制后又進(jìn)一步研究了C12orf29?!拔覀兪褂肅RISPR/Cas基因剪刀生成了一個(gè)人類腎細(xì)胞系,其中編碼C12orf29的基因被敲除。然后,我們能夠在不同的實(shí)驗(yàn)條件下將這些敲除(KO)細(xì)胞與‘正?!I細(xì)胞進(jìn)行比較,”Marx解釋說。
特別是,當(dāng)用K維生素甲萘醌處理細(xì)胞時(shí),KO細(xì)胞與具有功能性RNA連接酶的野生型細(xì)胞之間觀察到明顯的差異:相對(duì)低濃度的甲萘醌足以損傷KO細(xì)胞。相比之下,野生型細(xì)胞僅在明顯較高的濃度下受損。由于已知甲萘醌會(huì)引起氧化應(yīng)激,研究人員從這一結(jié)果中得出結(jié)論,C12orf29可以防止氧化細(xì)胞應(yīng)激。“我們假設(shè)以前隱藏的人類RNA修復(fù)機(jī)制是C12orf29生物學(xué)功能的基礎(chǔ)。我們現(xiàn)在需要在進(jìn)一步的研究中檢驗(yàn)這種機(jī)制,”Marx說。
這項(xiàng)研究是針對(duì)一種大腸桿菌菌株進(jìn)行的,這種細(xì)菌導(dǎo)致了大約80%的尿路感染,也是導(dǎo)致敗血癥的常見原因。臨床前試驗(yàn)證實(shí)了這一途徑在控制細(xì)菌感染中的作用。

圖2 RNA連接酶機(jī)制和用修飾的Ap3A探針通過化學(xué)蛋白質(zhì)組學(xué)鑒定C12orf29
研究總結(jié):
康斯坦茨的研究人員闡明了一種以前未被表征的人類蛋白質(zhì)(C12orf29)的功能。RNA連接酶催化了一種反應(yīng),這種反應(yīng)以前在人類中沒有發(fā)現(xiàn)過。這項(xiàng)研究的結(jié)果表明,在人類中存在一種以前被隱藏的RNA修復(fù)機(jī)制。
康斯坦茨大學(xué)化學(xué)系和生物系不同研究團(tuán)隊(duì)的跨學(xué)科合作項(xiàng)目
參考資料:
[1] Chemoproteomic discovery of a human RNA ligase
摘要:一種以前未被發(fā)現(xiàn)的蛋白質(zhì)的功能,在細(xì)胞應(yīng)激過程中對(duì)RNA修復(fù)很重要。。
核糖核酸(rna)是單鏈分子,在所有生物體的細(xì)胞中起著至關(guān)重要的作用。例如,作為我們基因的“轉(zhuǎn)錄本”,mRNA通過自己的序列攜帶制造蛋白質(zhì)的指令,參與了遺傳信息的翻譯??邓固勾拇髮W(xué)(University of Konstanz)有機(jī)和細(xì)胞化學(xué)教授Andreas Marx解釋說:“為了在細(xì)胞中發(fā)揮不同的功能,RNA通常需要進(jìn)行化學(xué)修飾,或在受損后進(jìn)行修復(fù)?!?/div>
圖1 蛋白質(zhì)C12orf29具有抵抗細(xì)胞應(yīng)激的保護(hù)功能
圖2 RNA連接酶機(jī)制和用修飾的Ap3A探針通過化學(xué)蛋白質(zhì)組學(xué)鑒定C12orf29
其中起作用的一種化學(xué)反應(yīng)是兩條RNA鏈在各自的兩端進(jìn)行三步連接(結(jié)扎)。這種反應(yīng)是由一種叫做RNA連接酶的特殊酶引發(fā)的,從病毒到真菌和植物,這種反應(yīng)存在于所有形式的生命中。在包括人類在內(nèi)的脊椎動(dòng)物中,這種RNA連接酶尚未被發(fā)現(xiàn)。來自康斯坦茨的一個(gè)跨學(xué)科研究小組現(xiàn)在發(fā)現(xiàn)了這種類型的第一個(gè)人類RNA連接酶:蛋白質(zhì)C12orf29。在細(xì)胞水平上,發(fā)表在《自然通訊》上的研究結(jié)果表明,這種酶具有抵抗細(xì)胞應(yīng)激的保護(hù)功能。

圖1 蛋白質(zhì)C12orf29具有抵抗細(xì)胞應(yīng)激的保護(hù)功能
“我們?cè)趯?duì)人類肺癌和腎細(xì)胞的廣泛研究中注意到C12orf29,我們?cè)趯ふ揖哂刑囟ɑ瘜W(xué)特征的蛋白質(zhì)時(shí)使用了新的化學(xué)工具。它引起了我們的注意,因?yàn)樵谀侵埃藗冞€不知道這種蛋白質(zhì)的功能是什么,”因此,研究人員開發(fā)并使用了各種方案來純化和預(yù)測(cè)未開發(fā)蛋白質(zhì)的結(jié)構(gòu),并進(jìn)行實(shí)驗(yàn)來追蹤其化學(xué)功能。因此,他們能夠證明最初只是一個(gè)合理的懷疑:C12orf29使用三磷酸腺苷(ATP)連接RNA鏈。
研究人員能夠詳細(xì)地展示這個(gè)過程遵循一個(gè)特征,從其他生命形式的其他RNA連接酶中已知的三步反應(yīng)模式。為了進(jìn)一步了解C12orf29在細(xì)胞水平上的功能,研究人員在闡明了化學(xué)機(jī)制后又進(jìn)一步研究了C12orf29?!拔覀兪褂肅RISPR/Cas基因剪刀生成了一個(gè)人類腎細(xì)胞系,其中編碼C12orf29的基因被敲除。然后,我們能夠在不同的實(shí)驗(yàn)條件下將這些敲除(KO)細(xì)胞與‘正?!I細(xì)胞進(jìn)行比較,”Marx解釋說。
特別是,當(dāng)用K維生素甲萘醌處理細(xì)胞時(shí),KO細(xì)胞與具有功能性RNA連接酶的野生型細(xì)胞之間觀察到明顯的差異:相對(duì)低濃度的甲萘醌足以損傷KO細(xì)胞。相比之下,野生型細(xì)胞僅在明顯較高的濃度下受損。由于已知甲萘醌會(huì)引起氧化應(yīng)激,研究人員從這一結(jié)果中得出結(jié)論,C12orf29可以防止氧化細(xì)胞應(yīng)激?!拔覀兗僭O(shè)以前隱藏的人類RNA修復(fù)機(jī)制是C12orf29生物學(xué)功能的基礎(chǔ)。我們現(xiàn)在需要在進(jìn)一步的研究中檢驗(yàn)這種機(jī)制,”Marx說。
這項(xiàng)研究是針對(duì)一種大腸桿菌菌株進(jìn)行的,這種細(xì)菌導(dǎo)致了大約80%的尿路感染,也是導(dǎo)致敗血癥的常見原因。臨床前試驗(yàn)證實(shí)了這一途徑在控制細(xì)菌感染中的作用。

圖2 RNA連接酶機(jī)制和用修飾的Ap3A探針通過化學(xué)蛋白質(zhì)組學(xué)鑒定C12orf29
研究總結(jié):
康斯坦茨的研究人員闡明了一種以前未被表征的人類蛋白質(zhì)(C12orf29)的功能。RNA連接酶催化了一種反應(yīng),這種反應(yīng)以前在人類中沒有發(fā)現(xiàn)過。這項(xiàng)研究的結(jié)果表明,在人類中存在一種以前被隱藏的RNA修復(fù)機(jī)制。
康斯坦茨大學(xué)化學(xué)系和生物系不同研究團(tuán)隊(duì)的跨學(xué)科合作項(xiàng)目
參考資料:
[1] Chemoproteomic discovery of a human RNA ligase



