隨著全球肥胖癥的日益嚴(yán)重,含人工甜味劑的「無糖飲料」越來越受到廣大消費(fèi)者的青睞。它們被宣傳只含有很少的熱量甚至零熱量,不僅滿足了消費(fèi)者對甜味的渴望,而且還不用擔(dān)心會發(fā)胖,因此深受大家的喜愛。然而,這可能僅僅是一場空歡喜。
2021年9月28日,發(fā)表在JAMA Network Open上的一項研究,來自美國南加州大學(xué)凱克醫(yī)學(xué)院領(lǐng)導(dǎo)的研究團(tuán)隊,發(fā)現(xiàn)女性和肥胖者可能對人工甜味劑更加敏感。這就意味著人工甜味飲料反而會讓他們感到饑餓,食欲大開,吃得更多,從而導(dǎo)致體重增加。

研究團(tuán)隊發(fā)現(xiàn)女性和肥胖者可能對人工甜味劑更加敏感
大量研究表明,人類和動物更喜歡營養(yǎng)糖,而不是無熱量的甜味劑。二十年前,在小鼠口中發(fā)現(xiàn)甜味感受器后不久,科學(xué)家們試圖敲除這些味蕾,但令人驚訝的是,即使沒有味覺,老鼠仍然能以某種方式辨別天然糖,而且他們更喜歡天然糖,而不是人造甜味劑。那么為什么人造甜味劑不能抑制人們對糖的渴望呢?近期的研究,為我們揭開了這個謎題的答案。
2022年1月13日,來自美國杜克大學(xué)的Diego V. Bohórquez團(tuán)隊在Nature Neuroscience雜志上發(fā)表了題為“The preference for sugar over sweetener depends on a gut sensor cell”的研究性論文,發(fā)現(xiàn)一種稱為Neuropod的腸道細(xì)胞,可以區(qū)分真糖和人造甜味劑,并且可以將差異以毫秒為單位傳達(dá)給你的大腦。

研究成果(圖源:Nature Neuroscience)
研究背景
腸內(nèi)分泌細(xì)胞中有一種腸感官上皮細(xì)胞,這種細(xì)胞可以和迷走神經(jīng)細(xì)胞產(chǎn)生突觸信號,形成神經(jīng)回路,這個腸內(nèi)分泌細(xì)胞就是Neuropod細(xì)胞,可以通過形成神經(jīng)回路將腸道和大腦直接連接起來。
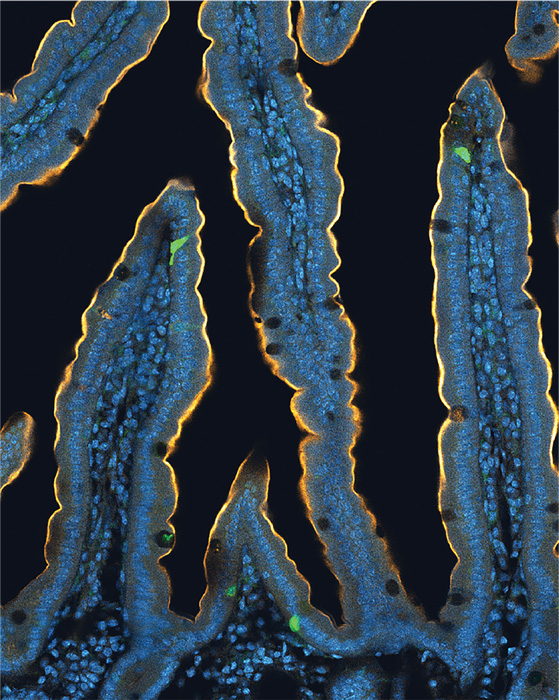
綠色熒光標(biāo)記的為腸道上皮中的Neuropod細(xì)胞(圖源:Borhóquez Lab, Duke University)
雖然感覺甜味取決于舌頭,但研究表明十二指腸也可以將糖分與甜味劑區(qū)分開來。蔗糖是 D-葡萄糖和 D-果糖組成的二糖。與 D-果糖或甜味劑三氯蔗糖不同,D-葡萄糖在十二指腸腔時會產(chǎn)生強(qiáng)烈的偏好。事實(shí)上,先前接觸過 D-葡萄糖的動物會在幾分鐘內(nèi)識別出進(jìn)入腸道的糖分。而當(dāng)繞過小腸時,這種識別 D-葡萄糖的能力就會消失,這表明十二指腸上皮是「糖傳感器」細(xì)胞所在的地方。但到目前為止,由于缺乏以時間和空間精度控制腸道感覺處理的工具,這些細(xì)胞的身份仍然難以識別。
研究內(nèi)容
迷走神經(jīng)對糖和甜味劑有反應(yīng)
研究者首先評估了灌注到近端小腸中的各種糖、糖類似物和無熱量甜味劑是否會引起快速的迷走神經(jīng)反應(yīng)。已知迷走神經(jīng)對蔗糖有反應(yīng),但對食物中常見的其他糖和甜味劑的反應(yīng)尚不清楚。
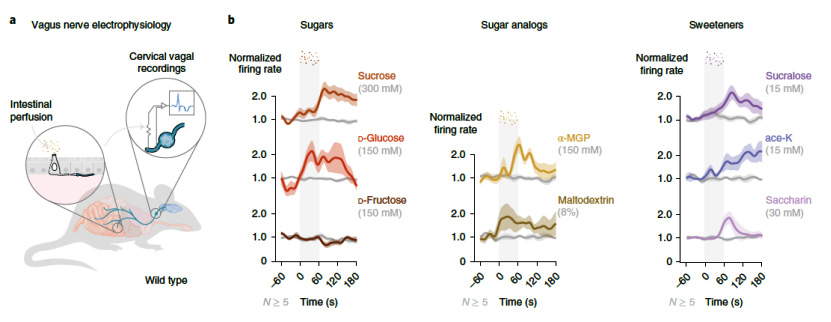
實(shí)驗(yàn)中評估了蔗糖(300 mM)、D-葡萄糖(150 mM)、D-果糖(150 mM)和 D-半乳糖(150 mM)、多種糖類似物 [甲基 α-D-吡喃葡萄糖苷(α- MGP;150 mM)、麥芽糖糊精(8%)和甜味劑三氯蔗糖(15 mM)、乙?;前匪徕洠?5 mM)和糖精(30 mM)] 的迷走神經(jīng)反應(yīng),記錄迷走神經(jīng)放電率。
所有糖都通過近端十二指腸灌注,繞過味覺或胃激活。使用放置在頸迷走神經(jīng)上的電極記錄神經(jīng)反應(yīng)。結(jié)果顯示在幾秒鐘內(nèi),幾乎所有的糖都會引起迷走神經(jīng)放電率的顯著增加。
(圖源:Nature Neuroscience)
迷走神經(jīng)反應(yīng)取決于十二指腸Neuropod細(xì)胞
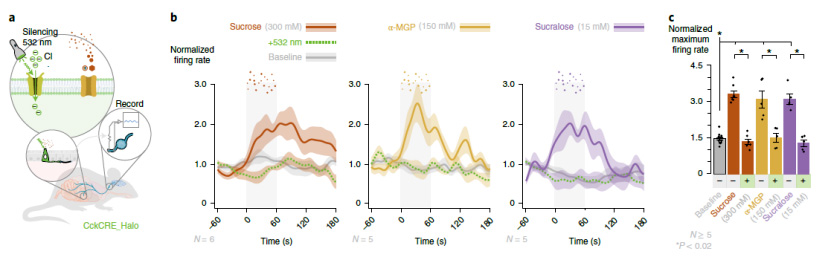
研究者假設(shè)迷走神經(jīng)反應(yīng)取決于腸上皮發(fā)出的信號,為了驗(yàn)證該假設(shè),使用 Cre/loxP 重組,培育了CckCRE_Halo小鼠,具有氯離子泵功能的嗜鹽菌紫質(zhì)(halorhodopsin)在十二指腸上皮細(xì)胞中的膽囊收縮素(Cck)啟動子下表達(dá)。當(dāng)被532 nm光觸發(fā)時,halorhodopsin可以使細(xì)胞膜超極化,立即沉默電興奮細(xì)胞。
在CckCRE_Halo小鼠中,迷走神經(jīng)對腔內(nèi)蔗糖、α-MGP 和三氯蔗糖的反應(yīng)在對照473 nm光存在下保持不變。然而,在532 nm光刺激下,對相同刺激的迷走神經(jīng)反應(yīng)完全消失,表明迷走神經(jīng)反應(yīng)取決于十二指腸CCK 標(biāo)記的 Neuropod細(xì)胞。
(圖源:Nature Neuroscience)
十二指腸 Neuropod 細(xì)胞可辨別甜味劑和糖
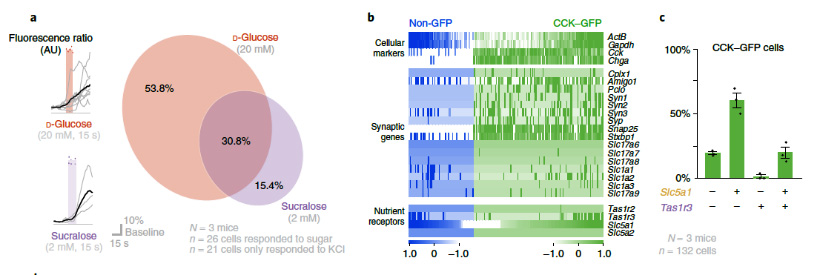
接下來,研究者檢測了單個CCK標(biāo)記的Neuropod細(xì)胞對糖和甜味劑的反應(yīng)。使用鈣指示染料Fluo-4和Fura Red在標(biāo)記有tdTomato(CckCRE_tdTomato)的單個 Neuropod細(xì)胞中對鈣瞬變進(jìn)行成像。陽性反應(yīng)定義為熒光比(Fluo-4/Fura Red)增加超過10%。在對至少一種糖有反應(yīng)的26個細(xì)胞中,53.8%的細(xì)胞僅對D-葡萄糖有反應(yīng),15.4%對三氯蔗糖有反應(yīng),30.8%對D-葡萄糖和三氯蔗糖都有反應(yīng)。
隨后,通過單細(xì)胞RT-qPCR在CCK-GFP和non-GFP腸上皮細(xì)胞中檢測基因表達(dá)。與non-GFP細(xì)胞相比,CCK-GFP細(xì)胞富含與突觸形成和囊泡功能或釋放相關(guān)的基因。此外,單個CCK-GFP細(xì)胞表達(dá)SGLT1和甜味受體。單個CCK-GFP細(xì)胞中的受體表達(dá)如下:Tas1r2可以忽略不計,Tas1r3單獨(dú)存在于1.2%的細(xì)胞中,SGLT1轉(zhuǎn)錄本Slc5a1單獨(dú)存在于60.1%的細(xì)胞中,并且Tas1r3和Slc5a1共存在于19.6%的細(xì)胞中。
那么,迷走神經(jīng)對糖或甜味劑的反應(yīng)是否由上皮SGLT或T1R3介導(dǎo)的呢?研究人員使用SGLT抑制劑 phloridzin,發(fā)現(xiàn)抑制SGLT后并不影響對三氯蔗糖的反應(yīng)。相反,阻斷包括T1R3在內(nèi)的甜味受體消除了對三氯蔗糖的迷走神經(jīng)反應(yīng),但不影響對蔗糖或α-MGP 的反應(yīng)。
在舌頭上的味覺轉(zhuǎn)導(dǎo)中,蔗糖和三氯蔗糖都可以激活T1R2/T1R3受體。但是,以上結(jié)果表明,在腸道中只有三氯蔗糖能引起味覺受體介導(dǎo)的迷走神經(jīng)反應(yīng)。這種差異可能是由于CCK標(biāo)記的Neuropod細(xì)胞中缺乏T1R2的表達(dá),這意味著腸道中的T1R3對三氯蔗糖比蔗糖更敏感。
(圖源:Nature Neuroscience)
糖而不是甜味劑會引發(fā)谷氨酸能神經(jīng)傳遞
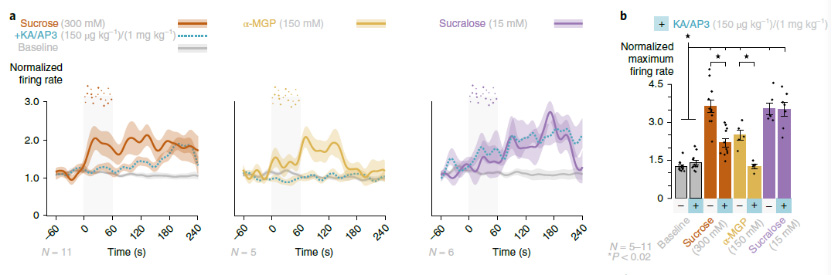
研究人員通過腔內(nèi)灌注犬尿酸(kynurenic acid, KA)和L-(+)-2-amino-3-phosphonopropionic acid(AP3),阻斷了離子型和代謝型谷氨酸受體,發(fā)現(xiàn)可以降低迷走神經(jīng)對蔗糖的早期反應(yīng),并完全減弱了對α-MGP的反應(yīng)。然而,谷氨酸抑制對三氯蔗糖的迷走神經(jīng)反應(yīng)并沒有受到影響。值得注意的是,抑制谷氨酸能神經(jīng)傳遞消除了α-MGP 的反應(yīng)。因此表明,糖進(jìn)入細(xì)胞后,會驅(qū)動Neuropod細(xì)胞和迷走神經(jīng)元之間的谷氨酸能神經(jīng)傳遞。
(圖源:Nature Neuroscience)
糖偏好取決于十二指腸 Neuropod 細(xì)胞
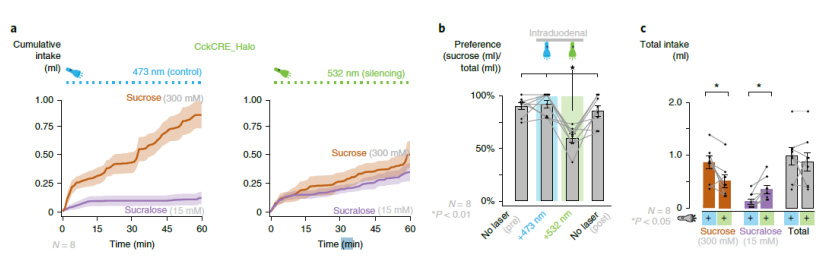
后續(xù),研究者試圖確定CCK標(biāo)記的Neuropod細(xì)胞對于小鼠辨別蔗糖和三氯蔗糖是否是必需的。他們通過使用光遺傳學(xué)的技術(shù),在小鼠腸道中植入柔性光纖,用于打開和關(guān)閉活體小鼠腸道的Neuropod細(xì)胞,以顯示動物對真正糖的偏好是否是由腸道信號驅(qū)動的。
結(jié)果顯示,在存在532 nm光的情況下,即沉默Neuropod細(xì)胞時,對照同窩小鼠表現(xiàn)出 90.8%的蔗糖偏好,而在CckCRE_Halo小鼠中,蔗糖偏好只有58.9%。重要的是,沉默 CCK標(biāo)記的Neuropod細(xì)胞會降低蔗糖攝入量,并增加三氯蔗糖攝入量,但1小時檢測期間,液體的總消耗量不受影響。換句話說,Neuropod細(xì)胞關(guān)閉,小鼠不再對真正的糖表現(xiàn)出明顯的偏好,證明小鼠對糖的偏好取決于Neuropod細(xì)胞。
(圖源:Nature Neuroscience)
總結(jié)
本研究表明小鼠對糖而不是甜味劑的偏好,取決于腸道中Neuropod細(xì)胞,它會釋放不同的神經(jīng)遞質(zhì)進(jìn)入迷走神經(jīng),進(jìn)而讓大腦區(qū)分糖和甜味劑。通過快速識別營養(yǎng)刺激的精確特性,腸道Neuropod細(xì)胞可作為指導(dǎo)營養(yǎng)選擇的切入點(diǎn)。
本文的通訊作者Bohórquez表示,Neuropod細(xì)胞是神經(jīng)系統(tǒng)的感覺細(xì)胞,就像舌頭中的味蕾幫助我們品嘗味道,或是像眼睛中的視網(wǎng)膜視錐細(xì)胞一樣,可以幫助我們看到顏色。它們感覺到糖與甜味劑的區(qū)別,然后釋放出不同的神經(jīng)遞質(zhì),這些神經(jīng)遞質(zhì)進(jìn)入迷走神經(jīng)中的不同細(xì)胞,動物知道「這是糖」或「這是甜味劑」。
「許多人都在為渴望糖而苦苦掙扎,現(xiàn)在我們對腸道如何感知糖,以及人造甜味劑為何不能抑制人們對糖的渴望,有了更好的了解,我們希望針對這個回路來治療相關(guān)疾病?!?,本研究的共同第一作者Kelly Buchanan說。
參考資料:
[1]Buchanan, K.L., Rupprecht, L.E., Kaelberer, M.M. et al. The preference for sugar over sweetener depends on a gut sensor cell. Nat Neurosci (2022). https://doi.org/10.1038/s41593-021-00982-7
隨著全球肥胖癥的日益嚴(yán)重,含人工甜味劑的「無糖飲料」越來越受到廣大消費(fèi)者的青睞。它們被宣傳只含有很少的熱量甚至零熱量,不僅滿足了消費(fèi)者對甜味的渴望,而且還不用擔(dān)心會發(fā)胖,因此深受大家的喜愛。然而,這可能僅僅是一場空歡喜。
2021年9月28日,發(fā)表在JAMA Network Open上的一項研究,來自美國南加州大學(xué)凱克醫(yī)學(xué)院領(lǐng)導(dǎo)的研究團(tuán)隊,發(fā)現(xiàn)女性和肥胖者可能對人工甜味劑更加敏感。這就意味著人工甜味飲料反而會讓他們感到饑餓,食欲大開,吃得更多,從而導(dǎo)致體重增加。

研究團(tuán)隊發(fā)現(xiàn)女性和肥胖者可能對人工甜味劑更加敏感
大量研究表明,人類和動物更喜歡營養(yǎng)糖,而不是無熱量的甜味劑。二十年前,在小鼠口中發(fā)現(xiàn)甜味感受器后不久,科學(xué)家們試圖敲除這些味蕾,但令人驚訝的是,即使沒有味覺,老鼠仍然能以某種方式辨別天然糖,而且他們更喜歡天然糖,而不是人造甜味劑。那么為什么人造甜味劑不能抑制人們對糖的渴望呢?近期的研究,為我們揭開了這個謎題的答案。
2022年1月13日,來自美國杜克大學(xué)的Diego V. Bohórquez團(tuán)隊在Nature Neuroscience雜志上發(fā)表了題為“The preference for sugar over sweetener depends on a gut sensor cell”的研究性論文,發(fā)現(xiàn)一種稱為Neuropod的腸道細(xì)胞,可以區(qū)分真糖和人造甜味劑,并且可以將差異以毫秒為單位傳達(dá)給你的大腦。

研究成果(圖源:Nature Neuroscience)
研究背景
腸內(nèi)分泌細(xì)胞中有一種腸感官上皮細(xì)胞,這種細(xì)胞可以和迷走神經(jīng)細(xì)胞產(chǎn)生突觸信號,形成神經(jīng)回路,這個腸內(nèi)分泌細(xì)胞就是Neuropod細(xì)胞,可以通過形成神經(jīng)回路將腸道和大腦直接連接起來。

綠色熒光標(biāo)記的為腸道上皮中的Neuropod細(xì)胞(圖源:Borhóquez Lab, Duke University)
雖然感覺甜味取決于舌頭,但研究表明十二指腸也可以將糖分與甜味劑區(qū)分開來。蔗糖是 D-葡萄糖和 D-果糖組成的二糖。與 D-果糖或甜味劑三氯蔗糖不同,D-葡萄糖在十二指腸腔時會產(chǎn)生強(qiáng)烈的偏好。事實(shí)上,先前接觸過 D-葡萄糖的動物會在幾分鐘內(nèi)識別出進(jìn)入腸道的糖分。而當(dāng)繞過小腸時,這種識別 D-葡萄糖的能力就會消失,這表明十二指腸上皮是「糖傳感器」細(xì)胞所在的地方。但到目前為止,由于缺乏以時間和空間精度控制腸道感覺處理的工具,這些細(xì)胞的身份仍然難以識別。
研究內(nèi)容
迷走神經(jīng)對糖和甜味劑有反應(yīng)
研究者首先評估了灌注到近端小腸中的各種糖、糖類似物和無熱量甜味劑是否會引起快速的迷走神經(jīng)反應(yīng)。已知迷走神經(jīng)對蔗糖有反應(yīng),但對食物中常見的其他糖和甜味劑的反應(yīng)尚不清楚。
實(shí)驗(yàn)中評估了蔗糖(300 mM)、D-葡萄糖(150 mM)、D-果糖(150 mM)和 D-半乳糖(150 mM)、多種糖類似物 [甲基 α-D-吡喃葡萄糖苷(α- MGP;150 mM)、麥芽糖糊精(8%)和甜味劑三氯蔗糖(15 mM)、乙酰磺胺酸鉀(15 mM)和糖精(30 mM)] 的迷走神經(jīng)反應(yīng),記錄迷走神經(jīng)放電率。
所有糖都通過近端十二指腸灌注,繞過味覺或胃激活。使用放置在頸迷走神經(jīng)上的電極記錄神經(jīng)反應(yīng)。結(jié)果顯示在幾秒鐘內(nèi),幾乎所有的糖都會引起迷走神經(jīng)放電率的顯著增加。

(圖源:Nature Neuroscience)
迷走神經(jīng)反應(yīng)取決于十二指腸Neuropod細(xì)胞
研究者假設(shè)迷走神經(jīng)反應(yīng)取決于腸上皮發(fā)出的信號,為了驗(yàn)證該假設(shè),使用 Cre/loxP 重組,培育了CckCRE_Halo小鼠,具有氯離子泵功能的嗜鹽菌紫質(zhì)(halorhodopsin)在十二指腸上皮細(xì)胞中的膽囊收縮素(Cck)啟動子下表達(dá)。當(dāng)被532 nm光觸發(fā)時,halorhodopsin可以使細(xì)胞膜超極化,立即沉默電興奮細(xì)胞。
在CckCRE_Halo小鼠中,迷走神經(jīng)對腔內(nèi)蔗糖、α-MGP 和三氯蔗糖的反應(yīng)在對照473 nm光存在下保持不變。然而,在532 nm光刺激下,對相同刺激的迷走神經(jīng)反應(yīng)完全消失,表明迷走神經(jīng)反應(yīng)取決于十二指腸CCK 標(biāo)記的 Neuropod細(xì)胞。

(圖源:Nature Neuroscience)
十二指腸 Neuropod 細(xì)胞可辨別甜味劑和糖
接下來,研究者檢測了單個CCK標(biāo)記的Neuropod細(xì)胞對糖和甜味劑的反應(yīng)。使用鈣指示染料Fluo-4和Fura Red在標(biāo)記有tdTomato(CckCRE_tdTomato)的單個 Neuropod細(xì)胞中對鈣瞬變進(jìn)行成像。陽性反應(yīng)定義為熒光比(Fluo-4/Fura Red)增加超過10%。在對至少一種糖有反應(yīng)的26個細(xì)胞中,53.8%的細(xì)胞僅對D-葡萄糖有反應(yīng),15.4%對三氯蔗糖有反應(yīng),30.8%對D-葡萄糖和三氯蔗糖都有反應(yīng)。
隨后,通過單細(xì)胞RT-qPCR在CCK-GFP和non-GFP腸上皮細(xì)胞中檢測基因表達(dá)。與non-GFP細(xì)胞相比,CCK-GFP細(xì)胞富含與突觸形成和囊泡功能或釋放相關(guān)的基因。此外,單個CCK-GFP細(xì)胞表達(dá)SGLT1和甜味受體。單個CCK-GFP細(xì)胞中的受體表達(dá)如下:Tas1r2可以忽略不計,Tas1r3單獨(dú)存在于1.2%的細(xì)胞中,SGLT1轉(zhuǎn)錄本Slc5a1單獨(dú)存在于60.1%的細(xì)胞中,并且Tas1r3和Slc5a1共存在于19.6%的細(xì)胞中。
那么,迷走神經(jīng)對糖或甜味劑的反應(yīng)是否由上皮SGLT或T1R3介導(dǎo)的呢?研究人員使用SGLT抑制劑 phloridzin,發(fā)現(xiàn)抑制SGLT后并不影響對三氯蔗糖的反應(yīng)。相反,阻斷包括T1R3在內(nèi)的甜味受體消除了對三氯蔗糖的迷走神經(jīng)反應(yīng),但不影響對蔗糖或α-MGP 的反應(yīng)。
在舌頭上的味覺轉(zhuǎn)導(dǎo)中,蔗糖和三氯蔗糖都可以激活T1R2/T1R3受體。但是,以上結(jié)果表明,在腸道中只有三氯蔗糖能引起味覺受體介導(dǎo)的迷走神經(jīng)反應(yīng)。這種差異可能是由于CCK標(biāo)記的Neuropod細(xì)胞中缺乏T1R2的表達(dá),這意味著腸道中的T1R3對三氯蔗糖比蔗糖更敏感。

(圖源:Nature Neuroscience)
糖而不是甜味劑會引發(fā)谷氨酸能神經(jīng)傳遞
研究人員通過腔內(nèi)灌注犬尿酸(kynurenic acid, KA)和L-(+)-2-amino-3-phosphonopropionic acid(AP3),阻斷了離子型和代謝型谷氨酸受體,發(fā)現(xiàn)可以降低迷走神經(jīng)對蔗糖的早期反應(yīng),并完全減弱了對α-MGP的反應(yīng)。然而,谷氨酸抑制對三氯蔗糖的迷走神經(jīng)反應(yīng)并沒有受到影響。值得注意的是,抑制谷氨酸能神經(jīng)傳遞消除了α-MGP 的反應(yīng)。因此表明,糖進(jìn)入細(xì)胞后,會驅(qū)動Neuropod細(xì)胞和迷走神經(jīng)元之間的谷氨酸能神經(jīng)傳遞。

(圖源:Nature Neuroscience)
糖偏好取決于十二指腸 Neuropod 細(xì)胞
后續(xù),研究者試圖確定CCK標(biāo)記的Neuropod細(xì)胞對于小鼠辨別蔗糖和三氯蔗糖是否是必需的。他們通過使用光遺傳學(xué)的技術(shù),在小鼠腸道中植入柔性光纖,用于打開和關(guān)閉活體小鼠腸道的Neuropod細(xì)胞,以顯示動物對真正糖的偏好是否是由腸道信號驅(qū)動的。
結(jié)果顯示,在存在532 nm光的情況下,即沉默Neuropod細(xì)胞時,對照同窩小鼠表現(xiàn)出 90.8%的蔗糖偏好,而在CckCRE_Halo小鼠中,蔗糖偏好只有58.9%。重要的是,沉默 CCK標(biāo)記的Neuropod細(xì)胞會降低蔗糖攝入量,并增加三氯蔗糖攝入量,但1小時檢測期間,液體的總消耗量不受影響。換句話說,Neuropod細(xì)胞關(guān)閉,小鼠不再對真正的糖表現(xiàn)出明顯的偏好,證明小鼠對糖的偏好取決于Neuropod細(xì)胞。

(圖源:Nature Neuroscience)
總結(jié)
本研究表明小鼠對糖而不是甜味劑的偏好,取決于腸道中Neuropod細(xì)胞,它會釋放不同的神經(jīng)遞質(zhì)進(jìn)入迷走神經(jīng),進(jìn)而讓大腦區(qū)分糖和甜味劑。通過快速識別營養(yǎng)刺激的精確特性,腸道Neuropod細(xì)胞可作為指導(dǎo)營養(yǎng)選擇的切入點(diǎn)。
本文的通訊作者Bohórquez表示,Neuropod細(xì)胞是神經(jīng)系統(tǒng)的感覺細(xì)胞,就像舌頭中的味蕾幫助我們品嘗味道,或是像眼睛中的視網(wǎng)膜視錐細(xì)胞一樣,可以幫助我們看到顏色。它們感覺到糖與甜味劑的區(qū)別,然后釋放出不同的神經(jīng)遞質(zhì),這些神經(jīng)遞質(zhì)進(jìn)入迷走神經(jīng)中的不同細(xì)胞,動物知道「這是糖」或「這是甜味劑」。
「許多人都在為渴望糖而苦苦掙扎,現(xiàn)在我們對腸道如何感知糖,以及人造甜味劑為何不能抑制人們對糖的渴望,有了更好的了解,我們希望針對這個回路來治療相關(guān)疾病?!?,本研究的共同第一作者Kelly Buchanan說。
參考資料:
[1]Buchanan, K.L., Rupprecht, L.E., Kaelberer, M.M. et al. The preference for sugar over sweetener depends on a gut sensor cell. Nat Neurosci (2022). https://doi.org/10.1038/s41593-021-00982-7



