光吃不胖,是吃貨們永恒的追求。然而熱量第一定律告訴我們,吃太多,總是要胖的。令人激動(dòng)的是,近期科學(xué)家們找到了一種顛覆性的“燃脂”方法,或許無(wú)需藥理刺激,便能長(zhǎng)久地促進(jìn)脂肪燃燒。
當(dāng)?shù)貢r(shí)間5月27日,期刊《Cell》在線發(fā)布了一項(xiàng)由哥本哈根大學(xué)諾和諾德基金會(huì)基礎(chǔ)代謝研究中心領(lǐng)銜帶來(lái)的研究報(bào)告。文章指出,研究人員已經(jīng)發(fā)現(xiàn)了一個(gè)調(diào)動(dòng)棕色脂肪組織(BAT)的有效靶標(biāo),通過(guò)基因工程提高該基因在小鼠體內(nèi)的表達(dá)水平后,即使長(zhǎng)期暴露于高脂飲食下,小鼠也能免受代謝疾病困擾,享“瘦”美食,并且該方法還具有持久生效的潛力。

一條獨(dú)特的燃脂路徑
眾所周知,棕色脂肪組織(BAT)是燃脂“小能手”,能夠加快人體新陳代謝,促進(jìn)白色脂肪消耗,這一特點(diǎn)使其成為治療代謝性疾病的理想靶點(diǎn)。然而,BAT通常僅在寒冷環(huán)境下由β-腎上腺素受體(β-AR)激活而起作用,盡管科學(xué)家們一直在嘗試藥理激活β-AR從而促進(jìn)BAT燃燒,但是這類(lèi)方法卻存在著增加心率和血壓等副作用。
興奮性G蛋白(Gs)偶聯(lián)受體家族被證實(shí)是BAT激活的主要誘因,在脂肪產(chǎn)熱的急性期和適應(yīng)性期起調(diào)節(jié)作用。
在這項(xiàng)新研究中,研究人員通過(guò)qPCR陣列從小鼠體內(nèi)44種Gs偶聯(lián)受體中找到了冷誘導(dǎo)下表達(dá)較為顯著的Gpr3受體。有趣的是,與其他受體不同,Gpr3受體無(wú)需外在配體,其氨基末端(N-末端)就能賦予該受體信號(hào)轉(zhuǎn)導(dǎo)活性,這說(shuō)明,Gpr3可能將具有長(zhǎng)久的BAT激活效果。
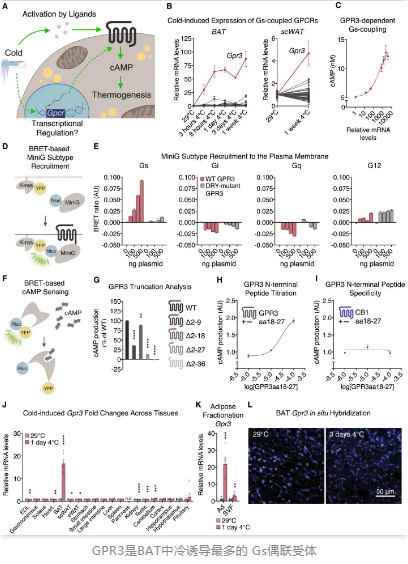
令人驚訝的是,Gpr3介導(dǎo)的BAT產(chǎn)熱似乎并不依賴(lài)β-AR路徑。在敲除了β-AR基因后,小鼠仍具有高表達(dá)的Gpr3,更為重要的是,Gpr3的過(guò)表達(dá)抑制了β-腎上腺素受體的表達(dá)。這些情況說(shuō)明,Gpr3是通過(guò)一種新的機(jī)制介導(dǎo)BAT產(chǎn)熱。
更安全、更燃脂、更長(zhǎng)效
當(dāng)然,關(guān)鍵問(wèn)題在于,這條新發(fā)現(xiàn)的通路是否具備更優(yōu)異的燃脂效果、更高的安全性和更好的臨床轉(zhuǎn)化可能性。
在進(jìn)一步試驗(yàn)中,研究人員通過(guò)基因工程改造和慢病毒誘導(dǎo)小鼠體內(nèi)Gpr3過(guò)表達(dá),結(jié)果發(fā)現(xiàn),此時(shí)BAT能耗更大,脂肪組織顯著減少,小鼠血糖得到更好的控制。同時(shí),與β-腎上腺素受體相比,GPR3引起的BAT活化更“偏愛(ài)”脂質(zhì)這一能耗來(lái)源。
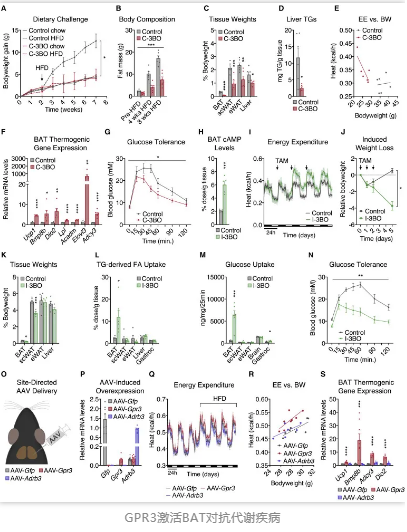
更為重要的是,提高棕色脂肪細(xì)胞中GPR3受體的表達(dá)水平能夠調(diào)節(jié)肥胖癥小鼠體內(nèi)的代謝穩(wěn)態(tài),幫助其恢復(fù)正常的代謝功能。這種效果并不需要長(zhǎng)期給藥才能實(shí)現(xiàn),研究人員發(fā)現(xiàn),僅需對(duì)小鼠注射一次攜帶GPR3的慢病毒顆粒,至少能夠維持1個(gè)多月的效果。
Gpr3在小鼠中表現(xiàn)出良好的BAT調(diào)控潛力,但是該靶點(diǎn)是否同樣適用于人體呢?研究人員評(píng)估了體重指數(shù)(BMI)和糖耐量水平不同的人類(lèi)志愿者的鎖骨BAT中GPR3基因的表達(dá),發(fā)現(xiàn)較高水平的BAT GPR3與較低的BMI顯著相關(guān),說(shuō)明人體內(nèi)GPR3的表達(dá)與全身代謝健康有關(guān)。
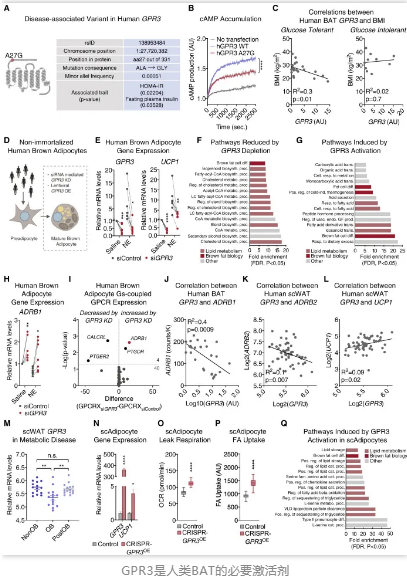
該報(bào)告的作者、哥本哈根大學(xué)諾和諾德基金會(huì)基礎(chǔ)代謝研究中心的Olivia Sveidahl Johansen博士說(shuō):“我們的研究表明,通過(guò)使用基因工具增加肥胖小鼠體內(nèi)GPR3的表達(dá),能夠減輕體重,恢復(fù)正常的血糖控制。GPR3激活了棕色脂肪細(xì)胞,將血液中的碳水化合物和脂質(zhì)全都消耗掉了。”
總之,這項(xiàng)研究揭示了一種激活BAT的全新路徑,GPR3是激活人BAT不可或缺的調(diào)節(jié)因子,具有長(zhǎng)久生效的潛力。目前,研究人員正在探索利用GPR3治療肥胖以及其他代謝性疾病的潛在策略。期待該方法能夠早日應(yīng)用于臨床!



