摘要:研究聚焦于腫瘤治療引發(fā)的腸道損傷修復(fù)難題,發(fā)現(xiàn)腸道局部調(diào)節(jié)性T細(xì)胞(Treg)在組織損傷后表達(dá)干擾素γ(IFN-γ)。
在腫瘤治療領(lǐng)域,化療、放療及免疫檢查點(diǎn)抑制劑等療法常引發(fā)嚴(yán)重的腸道損傷,成為限制治療效果的關(guān)鍵因素。這類(lèi)損傷不僅直接破壞腸上皮結(jié)構(gòu),更會(huì)觸發(fā)異常免疫反應(yīng),導(dǎo)致腸道屏障功能受損。其中,移植物抗宿主?。℅VHD)作為異基因造血干細(xì)胞移植(allo-HSCT)后的致命并發(fā)癥,其核心病理過(guò)程便涉及腸道上皮的嚴(yán)重?fù)p傷。長(zhǎng)期以來(lái),干擾素γ(IFN-γ)被視為腸道損傷的“罪魁禍?zhǔn)住?,研究表明活化的T細(xì)胞通過(guò)IFN-γ直接殺傷腸道干細(xì)胞(ISC),加劇組織損傷。然而,這一觀點(diǎn)難以解釋某些矛盾現(xiàn)象——例如,缺乏IFN-γ的移植模型反而出現(xiàn)更嚴(yán)重的腸道屏障破壞和死亡率。這種矛盾提示,IFN-γ在腸道損傷與修復(fù)中可能扮演著更為復(fù)雜的雙重角色。
為解決這一矛盾,由Julius C. Fischer、Sascha Gottert等學(xué)者組成的研究團(tuán)隊(duì)在《Signal Transduction and Targeted Therapy》發(fā)表研究,揭示了組織定居的調(diào)節(jié)性T細(xì)胞(Treg)通過(guò)協(xié)同提供IFN-γ和IL-10,巧妙地將炎癥信號(hào)轉(zhuǎn)化為再生信號(hào),從而驅(qū)動(dòng)腸道上皮修復(fù)的全新機(jī)制。

圖1 組織適應(yīng)性調(diào)節(jié)性T細(xì)胞駕馭炎性信號(hào)以促進(jìn)治療相關(guān)損傷后的腸道修復(fù)
研究人員綜合運(yùn)用小鼠異基因骨髓移植(allo-BMT)模型、腹部照射(ABI)模型、人源及鼠源腸道類(lèi)器官共培養(yǎng)系統(tǒng)、單細(xì)胞RNA測(cè)序(scRNA-seq)、芯片細(xì)胞術(shù)等多學(xué)科技術(shù)方法。研究納入了臨床allo-HSCT患者腸道活檢樣本進(jìn)行驗(yàn)證。通過(guò)體內(nèi)外模型結(jié)合多組學(xué)分析,系統(tǒng)闡述了Treg細(xì)胞來(lái)源的細(xì)胞因子對(duì)腸道干細(xì)胞行為的調(diào)控作用及分子機(jī)制。
Excessive intestinal tissue injury and regeneration are linked by IFN-γ and Treg cells
通過(guò)建立不同嚴(yán)重程度的allo-BMT模型,研究發(fā)現(xiàn)初始損傷越重,后續(xù)修復(fù)潛能越強(qiáng)。這種修復(fù)依賴(lài)于浸潤(rùn)T細(xì)胞產(chǎn)生的IFN-γ,因?yàn)镮FN-γ缺陷(Ifng-/-)的T細(xì)胞移植后,小鼠不僅死亡率增加,且腸道屏障功能恢復(fù)顯著延遲。同時(shí),損傷腸道中Treg細(xì)胞比例升高,而JAK1/2抑制劑魯索替尼(ruxolitinib)可通過(guò)進(jìn)一步增加Treg細(xì)胞浸潤(rùn),促進(jìn)腸道類(lèi)器官的再生能力。這些結(jié)果提示浸潤(rùn)的IFN-γ+ T細(xì)胞與Treg細(xì)胞共同參與修復(fù)過(guò)程。
Treg cell-mediated intestinal organoid growth requires epithelial IFN-γ receptor signaling
類(lèi)器官與T細(xì)胞共培養(yǎng)實(shí)驗(yàn)證實(shí),傳統(tǒng)T細(xì)胞(Tconv)抑制類(lèi)器官生長(zhǎng),而Treg細(xì)胞則促進(jìn)其生長(zhǎng)。這種促進(jìn)作用嚴(yán)格依賴(lài)于Treg細(xì)胞產(chǎn)生的IFN-γ和腸上皮細(xì)胞表達(dá)的IFN-γ受體(IFN-γR),因?yàn)槭褂肐FN-γ中和抗體或采用Ifngr1-/-類(lèi)器官均能消除該效應(yīng)。即使只有約5%的Treg細(xì)胞可檢測(cè)到IFN-γ蛋白,其促再生功能依然存在,提示低水平IFN-γ已足夠發(fā)揮作用。
Treg cell-mediated IL-10 and IFN-γ co-stimulation promotes murine and human intestinal organoid growth and repair from injury
研究發(fā)現(xiàn),低劑量重組IFN-γ(rIFN-γ)單獨(dú)使用并不能促進(jìn)類(lèi)器官生長(zhǎng),提示需要Treg細(xì)胞提供的第二信號(hào)。該信號(hào)被證實(shí)為IL-10。阻斷IL-10受體(IL-10R)或使用IFN-γ缺陷的Treg細(xì)胞,均完全消除了其促生長(zhǎng)作用。至關(guān)重要的是,只有IFN-γ和IL-10聯(lián)合刺激,才能有效促進(jìn)小鼠和人類(lèi)腸道類(lèi)器官的生長(zhǎng),并在體外照射后增強(qiáng)其再生。在腹部照射模型中,體內(nèi)阻斷IFN-γ或IL-10信號(hào)均會(huì)延緩恢復(fù),而雙信號(hào)阻斷則導(dǎo)致最嚴(yán)重的修復(fù)缺陷。值得注意的是,即使在損傷高峰期(體重最低點(diǎn))后開(kāi)始細(xì)胞因子阻斷,依然會(huì)損害修復(fù)過(guò)程,證明IFN-γ和IL-10在損傷后期同樣發(fā)揮關(guān)鍵的促再生作用。
Treg cells promote organoid growth via mTORC1 and Myc activation in ISCs
單細(xì)胞轉(zhuǎn)錄組分析揭示,Treg細(xì)胞共培養(yǎng)或IFN-γ/IL-10聯(lián)合刺激,顯著改變了腸道類(lèi)器官中干細(xì)胞(ISC)和短暫擴(kuò)增細(xì)胞(TA細(xì)胞)的基因表達(dá)譜,而未成熟分化細(xì)胞(如潘氏細(xì)胞、杯狀細(xì)胞)受影響較小?;蚣患治觯℅SEA)顯示,這兩種處理均特異性上調(diào)了ISC和TA細(xì)胞中的mTORC1和Myc信號(hào)通路。功能實(shí)驗(yàn)證實(shí),使用mTOR抑制劑雷帕霉素(rapamycin)或c-Myc抑制劑10058-F4可完全阻斷細(xì)胞因子或Treg細(xì)胞介導(dǎo)的類(lèi)器官生長(zhǎng)促進(jìn)作用,證明mTORC1和Myc是下游關(guān)鍵效應(yīng)器。
IFN-γ and IL-10 compensate for the depletion of epithelial growth factors
機(jī)制上,IFN-γ表現(xiàn)出類(lèi)似表皮生長(zhǎng)因子(EGF)的功能,能在EGF缺失條件下維持類(lèi)器官增殖和長(zhǎng)期培養(yǎng),該過(guò)程依賴(lài)mTOR和Myc信號(hào)。細(xì)胞周期分析顯示IFN-γ能快速驅(qū)動(dòng)上皮細(xì)胞進(jìn)入增殖周期,但長(zhǎng)期單獨(dú)使用會(huì)耗竭Lgr5+ ISC池。而IL-10則表現(xiàn)出類(lèi)似Wnt信號(hào)的特征,能在Wnt缺失條件下支持類(lèi)器官存活(尤其在人源類(lèi)器官中),并能拮抗IFN-γ對(duì)ISC的耗竭作用,兩者協(xié)同在促進(jìn)增殖的同時(shí)保障干細(xì)胞庫(kù)的維持。在急性損傷(如機(jī)械破壞)后,立即給予IFN-γ有害,而IL-10有益,再次凸顯了時(shí)機(jī)的重要性。體內(nèi)實(shí)驗(yàn)證實(shí),照射后IFN-γ確實(shí)驅(qū)動(dòng)了上皮細(xì)胞增殖,且未導(dǎo)致ISC池的即刻耗竭。
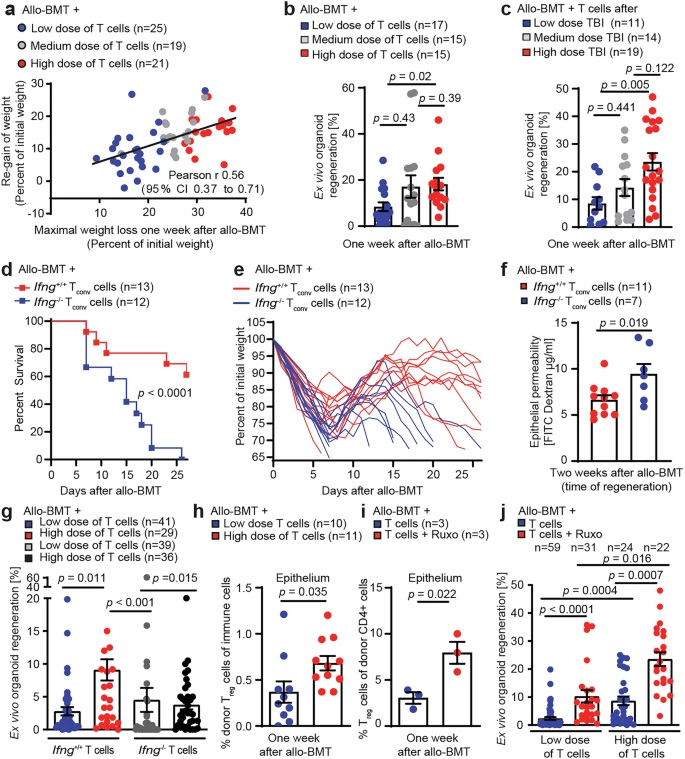
圖2 腸道組織的過(guò)度損傷與修復(fù)再生通過(guò)IFNγ和調(diào)節(jié)性T細(xì)胞形成雙向關(guān)聯(lián)
本研究結(jié)論性地揭示了腸道修復(fù)的一種新穎機(jī)制:組織適應(yīng)性Treg細(xì)胞通過(guò)協(xié)同提供IFN-γ和IL-10,經(jīng)mTORC1/Myc通路驅(qū)動(dòng)腸道干細(xì)胞介導(dǎo)的上皮再生。該發(fā)現(xiàn)革新了對(duì)IFN-γ在腸道炎癥中作用的認(rèn)識(shí),從單純的損傷因子轉(zhuǎn)變?yōu)楸尘耙蕾?lài)的、具有再生潛力的信號(hào)分子。同時(shí),它深化了對(duì)Treg細(xì)胞功能的理解,超越了其免疫抑制功能,突出了其直接促進(jìn)組織修復(fù)的能力。在轉(zhuǎn)化醫(yī)學(xué)層面,該研究為防治GVHD、放射性腸炎等治療相關(guān)腸道損傷提供了新的策略思路,例如通過(guò)調(diào)控局部細(xì)胞因子平衡或利用JAK抑制劑(如魯索替尼)富集具有再生功能的Treg細(xì)胞群體,從而在控制炎癥的同時(shí)主動(dòng)促進(jìn)黏膜修復(fù),最終改善腫瘤患者的治療耐受性和預(yù)后。
參考資料
[1] Tissue-adapted Tregs harness inflammatory signals to promote intestinal repair from therapy-related injury
摘要:研究聚焦于腫瘤治療引發(fā)的腸道損傷修復(fù)難題,發(fā)現(xiàn)腸道局部調(diào)節(jié)性T細(xì)胞(Treg)在組織損傷后表達(dá)干擾素γ(IFN-γ)。
在腫瘤治療領(lǐng)域,化療、放療及免疫檢查點(diǎn)抑制劑等療法常引發(fā)嚴(yán)重的腸道損傷,成為限制治療效果的關(guān)鍵因素。這類(lèi)損傷不僅直接破壞腸上皮結(jié)構(gòu),更會(huì)觸發(fā)異常免疫反應(yīng),導(dǎo)致腸道屏障功能受損。其中,移植物抗宿主?。℅VHD)作為異基因造血干細(xì)胞移植(allo-HSCT)后的致命并發(fā)癥,其核心病理過(guò)程便涉及腸道上皮的嚴(yán)重?fù)p傷。長(zhǎng)期以來(lái),干擾素γ(IFN-γ)被視為腸道損傷的“罪魁禍?zhǔn)住?,研究表明活化的T細(xì)胞通過(guò)IFN-γ直接殺傷腸道干細(xì)胞(ISC),加劇組織損傷。然而,這一觀點(diǎn)難以解釋某些矛盾現(xiàn)象——例如,缺乏IFN-γ的移植模型反而出現(xiàn)更嚴(yán)重的腸道屏障破壞和死亡率。這種矛盾提示,IFN-γ在腸道損傷與修復(fù)中可能扮演著更為復(fù)雜的雙重角色。
為解決這一矛盾,由Julius C. Fischer、Sascha Gottert等學(xué)者組成的研究團(tuán)隊(duì)在《Signal Transduction and Targeted Therapy》發(fā)表研究,揭示了組織定居的調(diào)節(jié)性T細(xì)胞(Treg)通過(guò)協(xié)同提供IFN-γ和IL-10,巧妙地將炎癥信號(hào)轉(zhuǎn)化為再生信號(hào),從而驅(qū)動(dòng)腸道上皮修復(fù)的全新機(jī)制。

圖1 組織適應(yīng)性調(diào)節(jié)性T細(xì)胞駕馭炎性信號(hào)以促進(jìn)治療相關(guān)損傷后的腸道修復(fù)
研究人員綜合運(yùn)用小鼠異基因骨髓移植(allo-BMT)模型、腹部照射(ABI)模型、人源及鼠源腸道類(lèi)器官共培養(yǎng)系統(tǒng)、單細(xì)胞RNA測(cè)序(scRNA-seq)、芯片細(xì)胞術(shù)等多學(xué)科技術(shù)方法。研究納入了臨床allo-HSCT患者腸道活檢樣本進(jìn)行驗(yàn)證。通過(guò)體內(nèi)外模型結(jié)合多組學(xué)分析,系統(tǒng)闡述了Treg細(xì)胞來(lái)源的細(xì)胞因子對(duì)腸道干細(xì)胞行為的調(diào)控作用及分子機(jī)制。
Excessive intestinal tissue injury and regeneration are linked by IFN-γ and Treg cells
通過(guò)建立不同嚴(yán)重程度的allo-BMT模型,研究發(fā)現(xiàn)初始損傷越重,后續(xù)修復(fù)潛能越強(qiáng)。這種修復(fù)依賴(lài)于浸潤(rùn)T細(xì)胞產(chǎn)生的IFN-γ,因?yàn)镮FN-γ缺陷(Ifng-/-)的T細(xì)胞移植后,小鼠不僅死亡率增加,且腸道屏障功能恢復(fù)顯著延遲。同時(shí),損傷腸道中Treg細(xì)胞比例升高,而JAK1/2抑制劑魯索替尼(ruxolitinib)可通過(guò)進(jìn)一步增加Treg細(xì)胞浸潤(rùn),促進(jìn)腸道類(lèi)器官的再生能力。這些結(jié)果提示浸潤(rùn)的IFN-γ+ T細(xì)胞與Treg細(xì)胞共同參與修復(fù)過(guò)程。
Treg cell-mediated intestinal organoid growth requires epithelial IFN-γ receptor signaling
類(lèi)器官與T細(xì)胞共培養(yǎng)實(shí)驗(yàn)證實(shí),傳統(tǒng)T細(xì)胞(Tconv)抑制類(lèi)器官生長(zhǎng),而Treg細(xì)胞則促進(jìn)其生長(zhǎng)。這種促進(jìn)作用嚴(yán)格依賴(lài)于Treg細(xì)胞產(chǎn)生的IFN-γ和腸上皮細(xì)胞表達(dá)的IFN-γ受體(IFN-γR),因?yàn)槭褂肐FN-γ中和抗體或采用Ifngr1-/-類(lèi)器官均能消除該效應(yīng)。即使只有約5%的Treg細(xì)胞可檢測(cè)到IFN-γ蛋白,其促再生功能依然存在,提示低水平IFN-γ已足夠發(fā)揮作用。
Treg cell-mediated IL-10 and IFN-γ co-stimulation promotes murine and human intestinal organoid growth and repair from injury
研究發(fā)現(xiàn),低劑量重組IFN-γ(rIFN-γ)單獨(dú)使用并不能促進(jìn)類(lèi)器官生長(zhǎng),提示需要Treg細(xì)胞提供的第二信號(hào)。該信號(hào)被證實(shí)為IL-10。阻斷IL-10受體(IL-10R)或使用IFN-γ缺陷的Treg細(xì)胞,均完全消除了其促生長(zhǎng)作用。至關(guān)重要的是,只有IFN-γ和IL-10聯(lián)合刺激,才能有效促進(jìn)小鼠和人類(lèi)腸道類(lèi)器官的生長(zhǎng),并在體外照射后增強(qiáng)其再生。在腹部照射模型中,體內(nèi)阻斷IFN-γ或IL-10信號(hào)均會(huì)延緩恢復(fù),而雙信號(hào)阻斷則導(dǎo)致最嚴(yán)重的修復(fù)缺陷。值得注意的是,即使在損傷高峰期(體重最低點(diǎn))后開(kāi)始細(xì)胞因子阻斷,依然會(huì)損害修復(fù)過(guò)程,證明IFN-γ和IL-10在損傷后期同樣發(fā)揮關(guān)鍵的促再生作用。
Treg cells promote organoid growth via mTORC1 and Myc activation in ISCs
單細(xì)胞轉(zhuǎn)錄組分析揭示,Treg細(xì)胞共培養(yǎng)或IFN-γ/IL-10聯(lián)合刺激,顯著改變了腸道類(lèi)器官中干細(xì)胞(ISC)和短暫擴(kuò)增細(xì)胞(TA細(xì)胞)的基因表達(dá)譜,而未成熟分化細(xì)胞(如潘氏細(xì)胞、杯狀細(xì)胞)受影響較小?;蚣患治觯℅SEA)顯示,這兩種處理均特異性上調(diào)了ISC和TA細(xì)胞中的mTORC1和Myc信號(hào)通路。功能實(shí)驗(yàn)證實(shí),使用mTOR抑制劑雷帕霉素(rapamycin)或c-Myc抑制劑10058-F4可完全阻斷細(xì)胞因子或Treg細(xì)胞介導(dǎo)的類(lèi)器官生長(zhǎng)促進(jìn)作用,證明mTORC1和Myc是下游關(guān)鍵效應(yīng)器。
IFN-γ and IL-10 compensate for the depletion of epithelial growth factors
機(jī)制上,IFN-γ表現(xiàn)出類(lèi)似表皮生長(zhǎng)因子(EGF)的功能,能在EGF缺失條件下維持類(lèi)器官增殖和長(zhǎng)期培養(yǎng),該過(guò)程依賴(lài)mTOR和Myc信號(hào)。細(xì)胞周期分析顯示IFN-γ能快速驅(qū)動(dòng)上皮細(xì)胞進(jìn)入增殖周期,但長(zhǎng)期單獨(dú)使用會(huì)耗竭Lgr5+ ISC池。而IL-10則表現(xiàn)出類(lèi)似Wnt信號(hào)的特征,能在Wnt缺失條件下支持類(lèi)器官存活(尤其在人源類(lèi)器官中),并能拮抗IFN-γ對(duì)ISC的耗竭作用,兩者協(xié)同在促進(jìn)增殖的同時(shí)保障干細(xì)胞庫(kù)的維持。在急性損傷(如機(jī)械破壞)后,立即給予IFN-γ有害,而IL-10有益,再次凸顯了時(shí)機(jī)的重要性。體內(nèi)實(shí)驗(yàn)證實(shí),照射后IFN-γ確實(shí)驅(qū)動(dòng)了上皮細(xì)胞增殖,且未導(dǎo)致ISC池的即刻耗竭。

圖2 腸道組織的過(guò)度損傷與修復(fù)再生通過(guò)IFNγ和調(diào)節(jié)性T細(xì)胞形成雙向關(guān)聯(lián)
本研究結(jié)論性地揭示了腸道修復(fù)的一種新穎機(jī)制:組織適應(yīng)性Treg細(xì)胞通過(guò)協(xié)同提供IFN-γ和IL-10,經(jīng)mTORC1/Myc通路驅(qū)動(dòng)腸道干細(xì)胞介導(dǎo)的上皮再生。該發(fā)現(xiàn)革新了對(duì)IFN-γ在腸道炎癥中作用的認(rèn)識(shí),從單純的損傷因子轉(zhuǎn)變?yōu)楸尘耙蕾?lài)的、具有再生潛力的信號(hào)分子。同時(shí),它深化了對(duì)Treg細(xì)胞功能的理解,超越了其免疫抑制功能,突出了其直接促進(jìn)組織修復(fù)的能力。在轉(zhuǎn)化醫(yī)學(xué)層面,該研究為防治GVHD、放射性腸炎等治療相關(guān)腸道損傷提供了新的策略思路,例如通過(guò)調(diào)控局部細(xì)胞因子平衡或利用JAK抑制劑(如魯索替尼)富集具有再生功能的Treg細(xì)胞群體,從而在控制炎癥的同時(shí)主動(dòng)促進(jìn)黏膜修復(fù),最終改善腫瘤患者的治療耐受性和預(yù)后。
參考資料
[1] Tissue-adapted Tregs harness inflammatory signals to promote intestinal repair from therapy-related injury



