摘要:通過生化與冷凍電鏡技術(shù),揭示ZAK激酶在核糖體碰撞中的激活機制。
在細胞內(nèi),蛋白質(zhì)合成是一個高度調(diào)控的過程,它不僅涉及遺傳信息的準確傳遞,還與細胞的應(yīng)激反應(yīng)密切相關(guān)。當翻譯過程中出現(xiàn)障礙時,例如mRNA的損傷或營養(yǎng)缺乏,細胞內(nèi)的核糖體會暫時停滯,這種停滯會導(dǎo)致相鄰的核糖體發(fā)生碰撞。這種核糖體碰撞不僅是細胞內(nèi)質(zhì)量控制機制的觸發(fā)信號,還與廣泛的應(yīng)激信號通路相關(guān),其中MAP3K ZAK介導(dǎo)的應(yīng)激反應(yīng)(RSR)在細胞命運調(diào)控中起著關(guān)鍵作用。ZAK通過磷酸化下游的MAPKs(如p38和JNK)來啟動一系列細胞應(yīng)激反應(yīng),包括細胞周期停滯和細胞凋亡。

圖1 在碰撞核糖體處引發(fā)的ZAK激活
盡管ZAK在細胞應(yīng)激反應(yīng)中扮演重要角色,但其與核糖體的相互作用機制及其如何被激活仍不完全清楚。近期的研究通過結(jié)合生化實驗與冷凍電鏡技術(shù),揭示了ZAK與核糖體之間復(fù)雜的相互作用網(wǎng)絡(luò)。這些相互作用不僅決定了ZAK在正常條件下的穩(wěn)定結(jié)合,還決定了其在應(yīng)激條件下的激活。研究發(fā)現(xiàn),ZAK在核糖體上的結(jié)合和激活依賴于多個關(guān)鍵結(jié)構(gòu)域和蛋白相互作用位點,其中RACK1是一個重要的支架蛋白,能夠促進ZAK的激活。
ZAK的C端區(qū)域包含多個與核糖體結(jié)合的關(guān)鍵結(jié)構(gòu)域,如與核糖體蛋白eS27和ES7的相互作用位點,這些結(jié)構(gòu)域在未發(fā)生碰撞時就已經(jīng)與核糖體結(jié)合,可能起到“采樣”作用,即在未應(yīng)激狀態(tài)下,ZAK通過這些位點與核糖體的多個部分建立弱相互作用,以保持其在細胞內(nèi)的分布。然而,當發(fā)生核糖體碰撞時,ZAK的結(jié)構(gòu)域會重新排列,使其與RACK1的特定區(qū)域(如RIM和RIH)發(fā)生更緊密的結(jié)合,從而促進其SAM結(jié)構(gòu)域的二聚化。這種SAM結(jié)構(gòu)域的二聚化是ZAK激活的關(guān)鍵步驟,它可能通過結(jié)構(gòu)上的改變促進其自身磷酸化,進而引發(fā)下游信號通路的激活。
研究還發(fā)現(xiàn),ZAK的激活過程受到另一種核糖體結(jié)合蛋白SERBP1的負調(diào)控。SERBP1通過與RACK1的特定區(qū)域(FPxL motif)結(jié)合,與ZAK競爭RACK1的結(jié)合位點,從而防止ZAK在未發(fā)生碰撞時被激活。這一發(fā)現(xiàn)提示,SERBP1可能作為ZAK的天然抑制因子,確保ZAK僅在特定的應(yīng)激條件下被激活,從而避免不必要的細胞損傷。
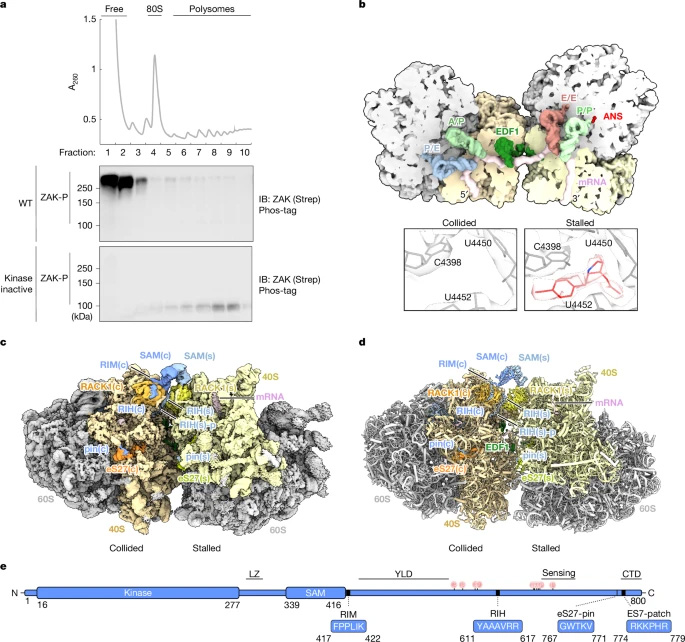
圖2 ZAKα蛋白結(jié)合碰撞二聚體核糖體的冷凍電鏡結(jié)構(gòu)
此外,研究還揭示了ZAK的SAM結(jié)構(gòu)域在核糖體碰撞后的關(guān)鍵作用。SAM結(jié)構(gòu)域的二聚化不僅促進ZAK的激活,還可能影響其與其他信號分子(如14-3-3蛋白)的相互作用,這些蛋白在ZAK激活后會幫助其招募到下游效應(yīng)器上,從而啟動應(yīng)激反應(yīng)。ZAK的某些突變形式,如F368C和W347S,表現(xiàn)出超活性,能夠在沒有核糖體碰撞的情況下激活ZAK,這表明SAM結(jié)構(gòu)域本身可能具有調(diào)控ZAK的活性和抑制功能。
研究中還通過不同實驗方法驗證了這些結(jié)構(gòu)域和相互作用位點的功能。例如,通過免疫印跡和CLIP-seq分析,研究人員確認了ZAK在核糖體上的結(jié)合模式及其在碰撞后的激活狀態(tài)。這些實驗不僅揭示了ZAK與核糖體的相互作用,還進一步說明了SAM結(jié)構(gòu)域的二聚化是ZAK激活的核心機制。
總體來看,這項研究為理解ZAK如何在核糖體碰撞后被激活提供了分子層面的藍圖。ZAK的激活過程涉及多個結(jié)構(gòu)域的協(xié)同作用,包括C端的結(jié)合位點、RIH和RIM的碰撞特異性相互作用,以及SAM結(jié)構(gòu)域的二聚化。這些相互作用共同構(gòu)成了一個精密的調(diào)控網(wǎng)絡(luò),確保ZAK在合適的時機被激活,從而引發(fā)細胞的應(yīng)激反應(yīng)。同時,研究還揭示了SERBP1在抑制ZAK激活中的作用,這為理解細胞如何在正常條件下維持ZAK的非激活狀態(tài)提供了重要線索。
此外,研究還探討了ZAK的活性調(diào)控是否依賴于核糖體。通過引入不同的突變體,研究人員發(fā)現(xiàn),某些SAM結(jié)構(gòu)域的突變可以繞過核糖體碰撞,直接導(dǎo)致ZAK的激活。這表明,ZAK的活性調(diào)控可能不僅僅依賴于核糖體的物理碰撞,而是通過其結(jié)構(gòu)域的相互作用來實現(xiàn)。這一發(fā)現(xiàn)為未來研究ZAK及其他SAM結(jié)構(gòu)域蛋白的調(diào)控機制提供了新的視角。
綜上所述,ZAK在細胞應(yīng)激反應(yīng)中的作用機制是復(fù)雜的,涉及多個結(jié)構(gòu)域與核糖體及其相關(guān)蛋白的相互作用。這些相互作用不僅決定了ZAK在細胞內(nèi)的分布和結(jié)合,還決定了其是否能夠被激活。
參考資料
[1] ZAK activation at the collided ribosome
摘要:通過生化與冷凍電鏡技術(shù),揭示ZAK激酶在核糖體碰撞中的激活機制。
在細胞內(nèi),蛋白質(zhì)合成是一個高度調(diào)控的過程,它不僅涉及遺傳信息的準確傳遞,還與細胞的應(yīng)激反應(yīng)密切相關(guān)。當翻譯過程中出現(xiàn)障礙時,例如mRNA的損傷或營養(yǎng)缺乏,細胞內(nèi)的核糖體會暫時停滯,這種停滯會導(dǎo)致相鄰的核糖體發(fā)生碰撞。這種核糖體碰撞不僅是細胞內(nèi)質(zhì)量控制機制的觸發(fā)信號,還與廣泛的應(yīng)激信號通路相關(guān),其中MAP3K ZAK介導(dǎo)的應(yīng)激反應(yīng)(RSR)在細胞命運調(diào)控中起著關(guān)鍵作用。ZAK通過磷酸化下游的MAPKs(如p38和JNK)來啟動一系列細胞應(yīng)激反應(yīng),包括細胞周期停滯和細胞凋亡。

圖1 在碰撞核糖體處引發(fā)的ZAK激活
盡管ZAK在細胞應(yīng)激反應(yīng)中扮演重要角色,但其與核糖體的相互作用機制及其如何被激活仍不完全清楚。近期的研究通過結(jié)合生化實驗與冷凍電鏡技術(shù),揭示了ZAK與核糖體之間復(fù)雜的相互作用網(wǎng)絡(luò)。這些相互作用不僅決定了ZAK在正常條件下的穩(wěn)定結(jié)合,還決定了其在應(yīng)激條件下的激活。研究發(fā)現(xiàn),ZAK在核糖體上的結(jié)合和激活依賴于多個關(guān)鍵結(jié)構(gòu)域和蛋白相互作用位點,其中RACK1是一個重要的支架蛋白,能夠促進ZAK的激活。
ZAK的C端區(qū)域包含多個與核糖體結(jié)合的關(guān)鍵結(jié)構(gòu)域,如與核糖體蛋白eS27和ES7的相互作用位點,這些結(jié)構(gòu)域在未發(fā)生碰撞時就已經(jīng)與核糖體結(jié)合,可能起到“采樣”作用,即在未應(yīng)激狀態(tài)下,ZAK通過這些位點與核糖體的多個部分建立弱相互作用,以保持其在細胞內(nèi)的分布。然而,當發(fā)生核糖體碰撞時,ZAK的結(jié)構(gòu)域會重新排列,使其與RACK1的特定區(qū)域(如RIM和RIH)發(fā)生更緊密的結(jié)合,從而促進其SAM結(jié)構(gòu)域的二聚化。這種SAM結(jié)構(gòu)域的二聚化是ZAK激活的關(guān)鍵步驟,它可能通過結(jié)構(gòu)上的改變促進其自身磷酸化,進而引發(fā)下游信號通路的激活。
研究還發(fā)現(xiàn),ZAK的激活過程受到另一種核糖體結(jié)合蛋白SERBP1的負調(diào)控。SERBP1通過與RACK1的特定區(qū)域(FPxL motif)結(jié)合,與ZAK競爭RACK1的結(jié)合位點,從而防止ZAK在未發(fā)生碰撞時被激活。這一發(fā)現(xiàn)提示,SERBP1可能作為ZAK的天然抑制因子,確保ZAK僅在特定的應(yīng)激條件下被激活,從而避免不必要的細胞損傷。

圖2 ZAKα蛋白結(jié)合碰撞二聚體核糖體的冷凍電鏡結(jié)構(gòu)
此外,研究還揭示了ZAK的SAM結(jié)構(gòu)域在核糖體碰撞后的關(guān)鍵作用。SAM結(jié)構(gòu)域的二聚化不僅促進ZAK的激活,還可能影響其與其他信號分子(如14-3-3蛋白)的相互作用,這些蛋白在ZAK激活后會幫助其招募到下游效應(yīng)器上,從而啟動應(yīng)激反應(yīng)。ZAK的某些突變形式,如F368C和W347S,表現(xiàn)出超活性,能夠在沒有核糖體碰撞的情況下激活ZAK,這表明SAM結(jié)構(gòu)域本身可能具有調(diào)控ZAK的活性和抑制功能。
研究中還通過不同實驗方法驗證了這些結(jié)構(gòu)域和相互作用位點的功能。例如,通過免疫印跡和CLIP-seq分析,研究人員確認了ZAK在核糖體上的結(jié)合模式及其在碰撞后的激活狀態(tài)。這些實驗不僅揭示了ZAK與核糖體的相互作用,還進一步說明了SAM結(jié)構(gòu)域的二聚化是ZAK激活的核心機制。
總體來看,這項研究為理解ZAK如何在核糖體碰撞后被激活提供了分子層面的藍圖。ZAK的激活過程涉及多個結(jié)構(gòu)域的協(xié)同作用,包括C端的結(jié)合位點、RIH和RIM的碰撞特異性相互作用,以及SAM結(jié)構(gòu)域的二聚化。這些相互作用共同構(gòu)成了一個精密的調(diào)控網(wǎng)絡(luò),確保ZAK在合適的時機被激活,從而引發(fā)細胞的應(yīng)激反應(yīng)。同時,研究還揭示了SERBP1在抑制ZAK激活中的作用,這為理解細胞如何在正常條件下維持ZAK的非激活狀態(tài)提供了重要線索。
此外,研究還探討了ZAK的活性調(diào)控是否依賴于核糖體。通過引入不同的突變體,研究人員發(fā)現(xiàn),某些SAM結(jié)構(gòu)域的突變可以繞過核糖體碰撞,直接導(dǎo)致ZAK的激活。這表明,ZAK的活性調(diào)控可能不僅僅依賴于核糖體的物理碰撞,而是通過其結(jié)構(gòu)域的相互作用來實現(xiàn)。這一發(fā)現(xiàn)為未來研究ZAK及其他SAM結(jié)構(gòu)域蛋白的調(diào)控機制提供了新的視角。
綜上所述,ZAK在細胞應(yīng)激反應(yīng)中的作用機制是復(fù)雜的,涉及多個結(jié)構(gòu)域與核糖體及其相關(guān)蛋白的相互作用。這些相互作用不僅決定了ZAK在細胞內(nèi)的分布和結(jié)合,還決定了其是否能夠被激活。
參考資料
[1] ZAK activation at the collided ribosome



