在蛋白質(zhì)組學(xué)、生物制藥開發(fā)及翻譯后修飾分析等前沿生物研究領(lǐng)域中,高特異性、高純度的工具酶發(fā)揮著不可或缺的關(guān)鍵作用。隨著重組DNA技術(shù)的不斷進(jìn)步,重組工具酶憑借其顯著性能優(yōu)勢(shì),正逐步取代傳統(tǒng)動(dòng)物源酶,成為科研探索與工業(yè)生產(chǎn)的核心試劑。
西寶生物布局高純度重組工具酶賽道,依托在重組蛋白技術(shù)領(lǐng)域的深厚積累,重點(diǎn)開發(fā)一系列高特異性、測(cè)序級(jí)別的重組工具酶產(chǎn)品。以卓越的批次間穩(wěn)定性和可擴(kuò)展性,滿足從基礎(chǔ)科研到大規(guī)模工業(yè)化生產(chǎn)對(duì)關(guān)鍵試劑日益增長(zhǎng)的需求,彰顯了公司賦能生物醫(yī)藥產(chǎn)業(yè)鏈的決心與實(shí)力。
一、蛋白酶類:蛋白質(zhì)酶解的核心工具
蛋白酶類的核心功能是將完整蛋白質(zhì)切割為適合分析的肽段,其切割特異性直接決定了酶解效果與后續(xù)分析的準(zhǔn)確性。
(一)測(cè)序級(jí)重組賴氨酰內(nèi)切酶(rLys-C)
作為絲氨酸蛋白酶,該酶具有極強(qiáng)的特異性,僅在賴氨酸殘基的 C 末端切割肽鍵。由于賴氨酸在蛋白質(zhì)中的出現(xiàn)頻率低于胰蛋白酶的主要切割位點(diǎn)(精氨酸 R 和賴氨酸 K),其酶解產(chǎn)物多為較長(zhǎng)肽段。在實(shí)際應(yīng)用中,rLys-C 常與胰蛋白酶聯(lián)用,先經(jīng) rLys-C 初步消化,再用胰蛋白酶進(jìn)一步切割,可顯著提升酶解覆蓋度,尤其適用于膜蛋白、難溶蛋白等難處理樣本的分析。此外,該酶還廣泛應(yīng)用于蛋白質(zhì)質(zhì)譜分析、胰島素類似物生產(chǎn)及肽圖譜制作。其重組表達(dá)特性賦予了無(wú)動(dòng)物源性污染,最適反應(yīng) pH 為 9.0-9.5。
(二)重組胰蛋白酶
胰蛋白酶是目前應(yīng)用最廣泛的蛋白質(zhì)酶解工具酶,特異性切割精氨酸(R)和賴氨酸(K)殘基的 C 末端肽鍵,且不切割被脯氨酸(P)緊隨其后的 R/K 位點(diǎn)。其酶解產(chǎn)生的肽段長(zhǎng)度多在 500-2500 Da 范圍內(nèi),完美匹配質(zhì)譜分析的需求。在蛋白質(zhì)組學(xué)、測(cè)序鑒定及翻譯后修飾分析中,胰蛋白酶均為優(yōu)選酶類。
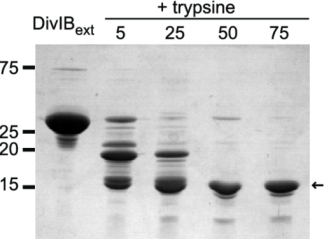
胰蛋白酶酶切DivIB胞外片段
(三)測(cè)序級(jí)重組糜蛋白酶
該酶為絲氨酸內(nèi)肽酶,選擇性切割Tyr/Phe/Trp殘基的 C 末端,最適 pH 為 7.0-9.0。與胰蛋白酶形成互補(bǔ),可提高富含疏水氨基酸區(qū)域的序列覆蓋度,生成重疊肽段用于從頭測(cè)序或序列確認(rèn),在蛋白質(zhì)組學(xué)研究中作為胰蛋白酶的補(bǔ)充工具。2-8℃條件下可穩(wěn)定 24 個(gè)月,適用于蛋白測(cè)序、抗體輕鏈分析等場(chǎng)景 。
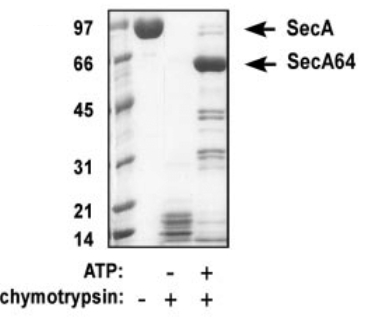
ATP添加下糜蛋白酶對(duì)SecA的不完全酶切
(四)重組羧肽酶 B(CPB)
測(cè)序級(jí)重組羧肽酶 B(CPB)是一種 Zn2?金屬蛋白酶,特異性從蛋白質(zhì)或肽的 C 末端依次切除堿性氨基酸(精氨酸 R、賴氨酸 K)。其核心應(yīng)用包括三個(gè)方面:一是 C 末端測(cè)序,與質(zhì)譜聯(lián)用通過監(jiān)測(cè)隨時(shí)間釋放的氨基酸可確定 C 末端序列;二是重組蛋白加工,去除表達(dá)產(chǎn)物 C 端額外帶有的精氨酸 / 賴氨酸(來自標(biāo)簽序列),實(shí)現(xiàn)蛋白的精準(zhǔn)修飾;三是胰島素前體加工研究,用于模擬生理加工過程。在實(shí)際應(yīng)用中,CPB 常用于抗體堿性峰檢測(cè)與 C 端序列分析,是生物制藥中蛋白精準(zhǔn)修飾的關(guān)鍵工具。
(五)重組 N - 糖苷酶 F(PNGase F)
糖基化是蛋白質(zhì)重要的翻譯后修飾,對(duì)蛋白質(zhì)的結(jié)構(gòu)與功能具有關(guān)鍵影響,而重組 N - 糖苷酶 F(PNGase F)是 N - 糖基化分析的核心工具酶。
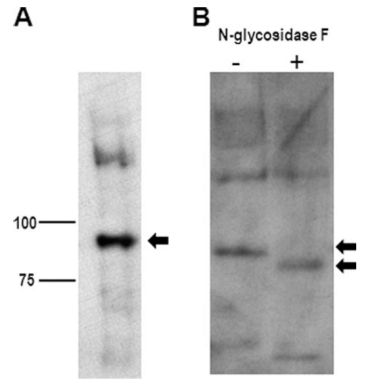
重組 N - 糖苷酶 F處理效果
PNGase F 能夠特異性水解天冬酰胺(Asn)與 N-聚糖之間的酰胺鍵,可裂解幾乎所有類型的哺乳動(dòng)物 N-聚糖,僅對(duì)核心 ɑ1-3 巖藻糖修飾的 N-聚糖無(wú)活性。其作用機(jī)制是將完整的糖鏈釋放,并將連接位點(diǎn)的天冬酰胺轉(zhuǎn)化為天冬氨酸(Asp)。這一特性為糖基化分析提供了多方面的支持:在去糖基化方面,PNGase F 能夠從糖蛋白上移除 N-聚糖,從而簡(jiǎn)化質(zhì)譜鑒定并提高酶解效率;在糖基化位點(diǎn)鑒定中,去糖基化導(dǎo)致原糖基化位點(diǎn)的 Asn 轉(zhuǎn)變?yōu)?Asp,在質(zhì)譜分析中引起質(zhì)量數(shù)增加,有助于精確定位修飾位點(diǎn);在聚糖結(jié)構(gòu)分析中,釋放出的完整聚糖可進(jìn)一步通過質(zhì)譜、HPLC 等技術(shù)解析其結(jié)構(gòu)。得益于重組表達(dá)技術(shù),PNGase F 已成為糖蛋白去糖基化、抗體糖型分析等研究中的關(guān)鍵工具酶。
(六)胃蛋白酶
作為酸性天冬氨酸蛋白酶,胃蛋白酶的切割位點(diǎn)較為廣泛,偏好疏水性氨基酸或芳香族氨基酸周圍的肽鍵,其最適活性 pH 為 1.0-5.0,在酸性條件下表現(xiàn)出優(yōu)異的穩(wěn)定性。核心應(yīng)用包括蛋白質(zhì)結(jié)構(gòu)分析(非變性條件下產(chǎn)生較大片段以研究結(jié)構(gòu)域)、抗體工程(制備抗體 F (ab') )、血清制品消化、疫苗生產(chǎn)及質(zhì)譜前處理。
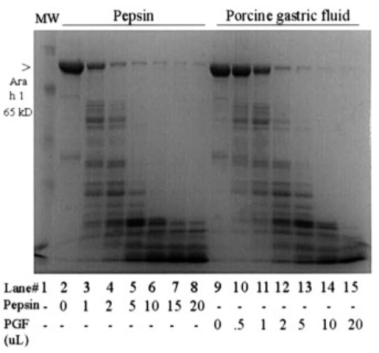
胃蛋白酶消化
詳詢西寶生物產(chǎn)品,請(qǐng)咨詢:400-021-8158 / 021-50272975。
貨號(hào) | CAS | 產(chǎn)品 |
EXK0369F | 72561-05-8 | 重組賴氨酰內(nèi)切酶(rLys-C) |
DCE0060Z | 9002-07-7 | 重組胰蛋白酶 |
| DYY0313E | 9004-07-3 | 重組糜蛋白酶 |
| DBY0114C | 9025-24-5 | 重組羧肽酶B |
ECE0441H | 83534-39-8 | 重組N-糖苷酶 F |
DCE0115J | 9001-75-6 | 胃蛋白酶(豬胃粘膜) |
二、應(yīng)用場(chǎng)景
蛋白質(zhì)組學(xué)研究:胰蛋白酶、rLys-C 及糜蛋白酶等多種蛋白酶可聯(lián)合使用,通過互補(bǔ)的酶切特性實(shí)現(xiàn)蛋白質(zhì)的高效、全面酶解,從而為質(zhì)譜分析提供覆蓋度更廣、質(zhì)量更高的肽段片段;
蛋白質(zhì)測(cè)序與鑒定:涵蓋 N 端、C 端及內(nèi)部肽段序列分析,常用 rLys-C、胰蛋白酶等進(jìn)行特異性酶切,結(jié)合羧肽酶 B 等工具酶輔助完成 C 端序列鑒定。
翻譯后修飾分析:PNGase F 用于 N-連接聚糖的去除,以解析 N-糖基化位點(diǎn)。
生物制藥:應(yīng)用于胰島素類似物的酶法制備、抗體工程(如 Fab 片段生成、糖基化表征)以及重組蛋白的精確酶促修飾等關(guān)鍵工藝步驟。
結(jié)構(gòu)生物學(xué)研究:胃蛋白酶可用于蛋白質(zhì)有限酶切,進(jìn)而分析其結(jié)構(gòu)域組成及研究蛋白質(zhì)構(gòu)象與折疊狀態(tài)。
參考
1. Soizic Masson, et al. Central Domain of DivIB Caps the C-terminal Regions of the FtsL/DivIC Coiled-coil Rod. DOI: 10.1074/jbc.M109.019471
2. A Price, et al. Separable ATPase and membrane insertion domains of the SecA subunit of preprotein translocase.J Biol Chem. 1996 Dec 6;271(49):31580-4
3. Randall A. Kopper, et al. Peanut protein allergens: Gastric digestion is carried out exclusively by pepsin. DOI: 10.1016/j.jaci.2004.05.012
4. Bianca C. Bernardo, et al. Cartilage Intermediate Layer Protein 2 (CILP-2) Is Expressed in Articular and Meniscal Cartilage and Down-regulated in Experimental Osteoarthritis. J Biol Chem. 2011 Oct 28;286(43):37758-67
在蛋白質(zhì)組學(xué)、生物制藥開發(fā)及翻譯后修飾分析等前沿生物研究領(lǐng)域中,高特異性、高純度的工具酶發(fā)揮著不可或缺的關(guān)鍵作用。隨著重組DNA技術(shù)的不斷進(jìn)步,重組工具酶憑借其顯著性能優(yōu)勢(shì),正逐步取代傳統(tǒng)動(dòng)物源酶,成為科研探索與工業(yè)生產(chǎn)的核心試劑。
西寶生物布局高純度重組工具酶賽道,依托在重組蛋白技術(shù)領(lǐng)域的深厚積累,重點(diǎn)開發(fā)一系列高特異性、測(cè)序級(jí)別的重組工具酶產(chǎn)品。以卓越的批次間穩(wěn)定性和可擴(kuò)展性,滿足從基礎(chǔ)科研到大規(guī)模工業(yè)化生產(chǎn)對(duì)關(guān)鍵試劑日益增長(zhǎng)的需求,彰顯了公司賦能生物醫(yī)藥產(chǎn)業(yè)鏈的決心與實(shí)力。
一、蛋白酶類:蛋白質(zhì)酶解的核心工具
蛋白酶類的核心功能是將完整蛋白質(zhì)切割為適合分析的肽段,其切割特異性直接決定了酶解效果與后續(xù)分析的準(zhǔn)確性。
(一)測(cè)序級(jí)重組賴氨酰內(nèi)切酶(rLys-C)
作為絲氨酸蛋白酶,該酶具有極強(qiáng)的特異性,僅在賴氨酸殘基的 C 末端切割肽鍵。由于賴氨酸在蛋白質(zhì)中的出現(xiàn)頻率低于胰蛋白酶的主要切割位點(diǎn)(精氨酸 R 和賴氨酸 K),其酶解產(chǎn)物多為較長(zhǎng)肽段。在實(shí)際應(yīng)用中,rLys-C 常與胰蛋白酶聯(lián)用,先經(jīng) rLys-C 初步消化,再用胰蛋白酶進(jìn)一步切割,可顯著提升酶解覆蓋度,尤其適用于膜蛋白、難溶蛋白等難處理樣本的分析。此外,該酶還廣泛應(yīng)用于蛋白質(zhì)質(zhì)譜分析、胰島素類似物生產(chǎn)及肽圖譜制作。其重組表達(dá)特性賦予了無(wú)動(dòng)物源性污染,最適反應(yīng) pH 為 9.0-9.5。
(二)重組胰蛋白酶
胰蛋白酶是目前應(yīng)用最廣泛的蛋白質(zhì)酶解工具酶,特異性切割精氨酸(R)和賴氨酸(K)殘基的 C 末端肽鍵,且不切割被脯氨酸(P)緊隨其后的 R/K 位點(diǎn)。其酶解產(chǎn)生的肽段長(zhǎng)度多在 500-2500 Da 范圍內(nèi),完美匹配質(zhì)譜分析的需求。在蛋白質(zhì)組學(xué)、測(cè)序鑒定及翻譯后修飾分析中,胰蛋白酶均為優(yōu)選酶類。

胰蛋白酶酶切DivIB胞外片段
(三)測(cè)序級(jí)重組糜蛋白酶
該酶為絲氨酸內(nèi)肽酶,選擇性切割Tyr/Phe/Trp殘基的 C 末端,最適 pH 為 7.0-9.0。與胰蛋白酶形成互補(bǔ),可提高富含疏水氨基酸區(qū)域的序列覆蓋度,生成重疊肽段用于從頭測(cè)序或序列確認(rèn),在蛋白質(zhì)組學(xué)研究中作為胰蛋白酶的補(bǔ)充工具。2-8℃條件下可穩(wěn)定 24 個(gè)月,適用于蛋白測(cè)序、抗體輕鏈分析等場(chǎng)景 。

ATP添加下糜蛋白酶對(duì)SecA的不完全酶切
(四)重組羧肽酶 B(CPB)
測(cè)序級(jí)重組羧肽酶 B(CPB)是一種 Zn2?金屬蛋白酶,特異性從蛋白質(zhì)或肽的 C 末端依次切除堿性氨基酸(精氨酸 R、賴氨酸 K)。其核心應(yīng)用包括三個(gè)方面:一是 C 末端測(cè)序,與質(zhì)譜聯(lián)用通過監(jiān)測(cè)隨時(shí)間釋放的氨基酸可確定 C 末端序列;二是重組蛋白加工,去除表達(dá)產(chǎn)物 C 端額外帶有的精氨酸 / 賴氨酸(來自標(biāo)簽序列),實(shí)現(xiàn)蛋白的精準(zhǔn)修飾;三是胰島素前體加工研究,用于模擬生理加工過程。在實(shí)際應(yīng)用中,CPB 常用于抗體堿性峰檢測(cè)與 C 端序列分析,是生物制藥中蛋白精準(zhǔn)修飾的關(guān)鍵工具。
(五)重組 N - 糖苷酶 F(PNGase F)
糖基化是蛋白質(zhì)重要的翻譯后修飾,對(duì)蛋白質(zhì)的結(jié)構(gòu)與功能具有關(guān)鍵影響,而重組 N - 糖苷酶 F(PNGase F)是 N - 糖基化分析的核心工具酶。

重組 N - 糖苷酶 F處理效果
PNGase F 能夠特異性水解天冬酰胺(Asn)與 N-聚糖之間的酰胺鍵,可裂解幾乎所有類型的哺乳動(dòng)物 N-聚糖,僅對(duì)核心 ɑ1-3 巖藻糖修飾的 N-聚糖無(wú)活性。其作用機(jī)制是將完整的糖鏈釋放,并將連接位點(diǎn)的天冬酰胺轉(zhuǎn)化為天冬氨酸(Asp)。這一特性為糖基化分析提供了多方面的支持:在去糖基化方面,PNGase F 能夠從糖蛋白上移除 N-聚糖,從而簡(jiǎn)化質(zhì)譜鑒定并提高酶解效率;在糖基化位點(diǎn)鑒定中,去糖基化導(dǎo)致原糖基化位點(diǎn)的 Asn 轉(zhuǎn)變?yōu)?Asp,在質(zhì)譜分析中引起質(zhì)量數(shù)增加,有助于精確定位修飾位點(diǎn);在聚糖結(jié)構(gòu)分析中,釋放出的完整聚糖可進(jìn)一步通過質(zhì)譜、HPLC 等技術(shù)解析其結(jié)構(gòu)。得益于重組表達(dá)技術(shù),PNGase F 已成為糖蛋白去糖基化、抗體糖型分析等研究中的關(guān)鍵工具酶。
(六)胃蛋白酶
作為酸性天冬氨酸蛋白酶,胃蛋白酶的切割位點(diǎn)較為廣泛,偏好疏水性氨基酸或芳香族氨基酸周圍的肽鍵,其最適活性 pH 為 1.0-5.0,在酸性條件下表現(xiàn)出優(yōu)異的穩(wěn)定性。核心應(yīng)用包括蛋白質(zhì)結(jié)構(gòu)分析(非變性條件下產(chǎn)生較大片段以研究結(jié)構(gòu)域)、抗體工程(制備抗體 F (ab') )、血清制品消化、疫苗生產(chǎn)及質(zhì)譜前處理。

胃蛋白酶消化
詳詢西寶生物產(chǎn)品,請(qǐng)咨詢:400-021-8158 / 021-50272975。
貨號(hào) | CAS | 產(chǎn)品 |
EXK0369F | 72561-05-8 | 重組賴氨酰內(nèi)切酶(rLys-C) |
DCE0060Z | 9002-07-7 | 重組胰蛋白酶 |
| DYY0313E | 9004-07-3 | 重組糜蛋白酶 |
| DBY0114C | 9025-24-5 | 重組羧肽酶B |
ECE0441H | 83534-39-8 | 重組N-糖苷酶 F |
DCE0115J | 9001-75-6 | 胃蛋白酶(豬胃粘膜) |
二、應(yīng)用場(chǎng)景
蛋白質(zhì)組學(xué)研究:胰蛋白酶、rLys-C 及糜蛋白酶等多種蛋白酶可聯(lián)合使用,通過互補(bǔ)的酶切特性實(shí)現(xiàn)蛋白質(zhì)的高效、全面酶解,從而為質(zhì)譜分析提供覆蓋度更廣、質(zhì)量更高的肽段片段;
蛋白質(zhì)測(cè)序與鑒定:涵蓋 N 端、C 端及內(nèi)部肽段序列分析,常用 rLys-C、胰蛋白酶等進(jìn)行特異性酶切,結(jié)合羧肽酶 B 等工具酶輔助完成 C 端序列鑒定。
翻譯后修飾分析:PNGase F 用于 N-連接聚糖的去除,以解析 N-糖基化位點(diǎn)。
生物制藥:應(yīng)用于胰島素類似物的酶法制備、抗體工程(如 Fab 片段生成、糖基化表征)以及重組蛋白的精確酶促修飾等關(guān)鍵工藝步驟。
結(jié)構(gòu)生物學(xué)研究:胃蛋白酶可用于蛋白質(zhì)有限酶切,進(jìn)而分析其結(jié)構(gòu)域組成及研究蛋白質(zhì)構(gòu)象與折疊狀態(tài)。
參考
1. Soizic Masson, et al. Central Domain of DivIB Caps the C-terminal Regions of the FtsL/DivIC Coiled-coil Rod. DOI: 10.1074/jbc.M109.019471
2. A Price, et al. Separable ATPase and membrane insertion domains of the SecA subunit of preprotein translocase.J Biol Chem. 1996 Dec 6;271(49):31580-4
3. Randall A. Kopper, et al. Peanut protein allergens: Gastric digestion is carried out exclusively by pepsin. DOI: 10.1016/j.jaci.2004.05.012
4. Bianca C. Bernardo, et al. Cartilage Intermediate Layer Protein 2 (CILP-2) Is Expressed in Articular and Meniscal Cartilage and Down-regulated in Experimental Osteoarthritis. J Biol Chem. 2011 Oct 28;286(43):37758-67



