摘要:研究人員發(fā)現(xiàn)了一種此前未知的機(jī)制,解釋了細(xì)菌如何導(dǎo)致口腔癌和結(jié)直腸癌患者產(chǎn)生治療耐藥性。
人們已在多種癌癥中發(fā)現(xiàn)腫瘤內(nèi)細(xì)菌,尤其是在黏膜部位,并將其視為腫瘤微環(huán)境的組成部分。然而,這些微生物如何影響微環(huán)境,目前仍不大清楚。
近日,F(xiàn)red Hutchinson癌癥中心和MD Anderson癌癥中心的研究人員發(fā)現(xiàn)了一種此前未知的機(jī)制,解釋了細(xì)菌如何導(dǎo)致口腔癌和結(jié)直腸癌患者產(chǎn)生治療耐藥性。這項成果于10月16日發(fā)表在《Cancer Cell》雜志上。
研究發(fā)現(xiàn),某些細(xì)菌,尤其是具核梭桿菌(Fn),會誘導(dǎo)癌癥上皮細(xì)胞進(jìn)入一種可逆狀態(tài),即靜息狀態(tài)。這使得腫瘤能夠逃避免疫系統(tǒng)的攻擊,并抵抗化療。
通訊作者、MD Anderson癌癥中心免疫學(xué)系副教授Susan Bullman博士表示:“這些細(xì)菌與腫瘤的相互作用一直隱藏在暗處。如今借助新技術(shù),我們可以觀察到微生物如何直接影響癌細(xì)胞、塑造腫瘤行為并削弱治療效果?!?/div>
圖1 腫瘤浸潤細(xì)菌破壞癌細(xì)胞間上皮相互作用并誘導(dǎo)細(xì)胞周期阻滯
圖1 腫瘤浸潤細(xì)菌破壞癌細(xì)胞間上皮相互作用并誘導(dǎo)細(xì)胞周期阻滯

圖1 腫瘤浸潤細(xì)菌破壞癌細(xì)胞間上皮相互作用并誘導(dǎo)細(xì)胞周期阻滯
“這是我們一直忽視的腫瘤生物學(xué)層面,而現(xiàn)在我們開始著手研究它。我們希望這些發(fā)現(xiàn)能協(xié)助人們設(shè)計出針對微生物的療法,讓最棘手的癌癥也能輕松治愈?!?/div>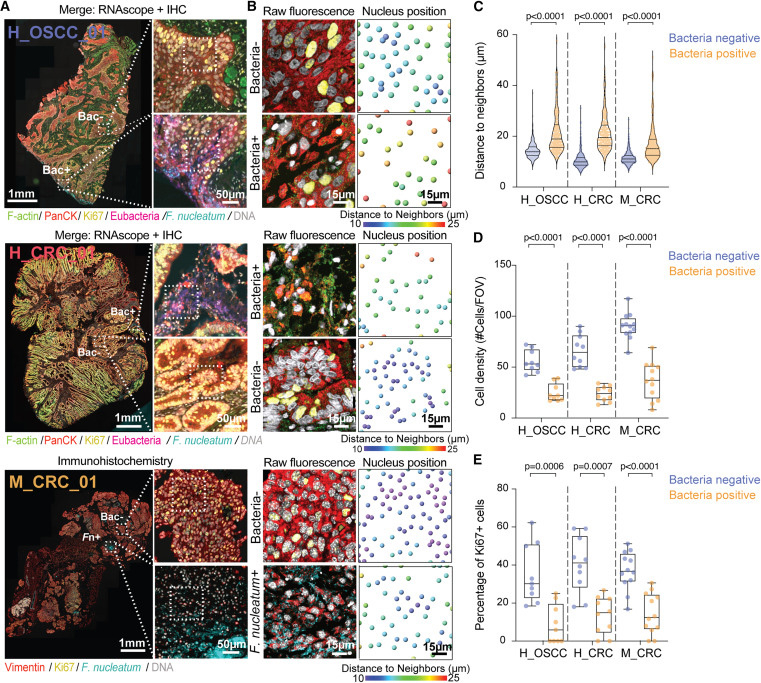
圖2 細(xì)菌感染微灶內(nèi)癌細(xì)胞的空間分布
在這項研究中,研究人員發(fā)現(xiàn)胞外的梭桿菌進(jìn)入腫瘤并包圍腫瘤上皮細(xì)胞,有效地切斷它們與周圍細(xì)胞的通訊,并使癌細(xì)胞暫時進(jìn)入靜息狀態(tài)。這反過來又使它們能夠逃避免疫系統(tǒng),抵抗化療并促進(jìn)轉(zhuǎn)移。
空間成像與空間轉(zhuǎn)錄組學(xué)分析顯示,梭桿菌主要定位在結(jié)直腸癌和口腔癌的腫瘤微環(huán)境中,該區(qū)域以細(xì)胞密度降低、轉(zhuǎn)錄活性減弱及增殖減慢為特征。
體外實驗表明,具核梭桿菌可破壞上皮細(xì)胞連接,誘導(dǎo)G0-G1期阻滯和轉(zhuǎn)錄靜息狀態(tài)。這種狀態(tài)
重塑腫瘤微環(huán)境,并使得細(xì)胞對化療藥物氟尿嘧啶(5-fluorouracil)產(chǎn)生耐藥性。
研究人員在52例結(jié)直腸癌患者隊列中驗證了這些發(fā)現(xiàn)。在一個獨立的患者隊列中,高水平的梭桿菌與抗原呈遞基因下調(diào)和療效下降顯著相關(guān)。

圖2 細(xì)菌感染微灶內(nèi)癌細(xì)胞的空間分布
這些發(fā)現(xiàn)將胞外細(xì)菌與癌細(xì)胞靜息與化療耐藥相關(guān)聯(lián),凸顯了以微生物-腫瘤相互作用為治療靶點的價值。
研究團(tuán)隊也在探索如何將靶向腫瘤的細(xì)菌改造成未來的治療工具。這種“以菌為藥”的方法在癌癥治療中大有前景,因為實體瘤通常對傳統(tǒng)療法具有耐藥性。
不過,研究人員也承認(rèn),研究的局限性在于,實驗條件(包括實驗室細(xì)菌劑量和氧氣水平)可能無法完全模擬人類腫瘤內(nèi)復(fù)雜而動態(tài)的環(huán)境。這凸顯了需要進(jìn)一步研究以便更好地了解體內(nèi)這些相互作用。
參考資料
[1] Tumor-infiltrating bacteria disrupt cancer epithelial cell interactions and induce cell-cycle arrest
摘要:研究人員發(fā)現(xiàn)了一種此前未知的機(jī)制,解釋了細(xì)菌如何導(dǎo)致口腔癌和結(jié)直腸癌患者產(chǎn)生治療耐藥性。
人們已在多種癌癥中發(fā)現(xiàn)腫瘤內(nèi)細(xì)菌,尤其是在黏膜部位,并將其視為腫瘤微環(huán)境的組成部分。然而,這些微生物如何影響微環(huán)境,目前仍不大清楚。
近日,F(xiàn)red Hutchinson癌癥中心和MD Anderson癌癥中心的研究人員發(fā)現(xiàn)了一種此前未知的機(jī)制,解釋了細(xì)菌如何導(dǎo)致口腔癌和結(jié)直腸癌患者產(chǎn)生治療耐藥性。這項成果于10月16日發(fā)表在《Cancer Cell》雜志上。
研究發(fā)現(xiàn),某些細(xì)菌,尤其是具核梭桿菌(Fn),會誘導(dǎo)癌癥上皮細(xì)胞進(jìn)入一種可逆狀態(tài),即靜息狀態(tài)。這使得腫瘤能夠逃避免疫系統(tǒng)的攻擊,并抵抗化療。
通訊作者、MD Anderson癌癥中心免疫學(xué)系副教授Susan Bullman博士表示:“這些細(xì)菌與腫瘤的相互作用一直隱藏在暗處。如今借助新技術(shù),我們可以觀察到微生物如何直接影響癌細(xì)胞、塑造腫瘤行為并削弱治療效果。”

圖1 腫瘤浸潤細(xì)菌破壞癌細(xì)胞間上皮相互作用并誘導(dǎo)細(xì)胞周期阻滯
“這是我們一直忽視的腫瘤生物學(xué)層面,而現(xiàn)在我們開始著手研究它。我們希望這些發(fā)現(xiàn)能協(xié)助人們設(shè)計出針對微生物的療法,讓最棘手的癌癥也能輕松治愈?!?/div>
圖2 細(xì)菌感染微灶內(nèi)癌細(xì)胞的空間分布
在這項研究中,研究人員發(fā)現(xiàn)胞外的梭桿菌進(jìn)入腫瘤并包圍腫瘤上皮細(xì)胞,有效地切斷它們與周圍細(xì)胞的通訊,并使癌細(xì)胞暫時進(jìn)入靜息狀態(tài)。這反過來又使它們能夠逃避免疫系統(tǒng),抵抗化療并促進(jìn)轉(zhuǎn)移。
空間成像與空間轉(zhuǎn)錄組學(xué)分析顯示,梭桿菌主要定位在結(jié)直腸癌和口腔癌的腫瘤微環(huán)境中,該區(qū)域以細(xì)胞密度降低、轉(zhuǎn)錄活性減弱及增殖減慢為特征。
體外實驗表明,具核梭桿菌可破壞上皮細(xì)胞連接,誘導(dǎo)G0-G1期阻滯和轉(zhuǎn)錄靜息狀態(tài)。這種狀態(tài)重塑腫瘤微環(huán)境,并使得細(xì)胞對化療藥物氟尿嘧啶(5-fluorouracil)產(chǎn)生耐藥性。
研究人員在52例結(jié)直腸癌患者隊列中驗證了這些發(fā)現(xiàn)。在一個獨立的患者隊列中,高水平的梭桿菌與抗原呈遞基因下調(diào)和療效下降顯著相關(guān)。

圖2 細(xì)菌感染微灶內(nèi)癌細(xì)胞的空間分布
這些發(fā)現(xiàn)將胞外細(xì)菌與癌細(xì)胞靜息與化療耐藥相關(guān)聯(lián),凸顯了以微生物-腫瘤相互作用為治療靶點的價值。
研究團(tuán)隊也在探索如何將靶向腫瘤的細(xì)菌改造成未來的治療工具。這種“以菌為藥”的方法在癌癥治療中大有前景,因為實體瘤通常對傳統(tǒng)療法具有耐藥性。
不過,研究人員也承認(rèn),研究的局限性在于,實驗條件(包括實驗室細(xì)菌劑量和氧氣水平)可能無法完全模擬人類腫瘤內(nèi)復(fù)雜而動態(tài)的環(huán)境。這凸顯了需要進(jìn)一步研究以便更好地了解體內(nèi)這些相互作用。
參考資料
[1] Tumor-infiltrating bacteria disrupt cancer epithelial cell interactions and induce cell-cycle arrest



