摘要:研究首次證實(shí)靶向CTNNB1S37F驅(qū)動(dòng)突變的TCR-T細(xì)胞能有效清除表達(dá)HLA-A02:01/HLA-A24:02的實(shí)體瘤。
HLA結(jié)合的復(fù)發(fā)驅(qū)動(dòng)突變肽段是T細(xì)胞免疫治療的潛在靶點(diǎn)。研究發(fā)現(xiàn)CTNNB1S37F突變產(chǎn)生的兩種新抗原肽可被HLA-A02:01和HLA-A24:02遞呈,該突變導(dǎo)致β-catenin功能增強(qiáng),美國(guó)每年新增病例超7,000例。從健康供體幼稚T細(xì)胞中分離出特異性TCR,轉(zhuǎn)導(dǎo)的T細(xì)胞在體外能有效殺傷CTNNB1S37F+細(xì)胞系和患者來(lái)源類(lèi)器官,并在黑色素瘤細(xì)胞系和小鼠子宮內(nèi)膜腺癌PDX模型中清除已形成的腫瘤。

圖1 靶向共享性β-連環(huán)蛋白突變的TCR工程化T細(xì)胞清除實(shí)體瘤
突變癌癥的流行率和發(fā)病率
分析MSK-MET研究25,775例樣本顯示,子宮內(nèi)膜癌(3.35%)、宮頸癌(2.91%)和小腸癌(1.06%)中CTNNB1S37F突變頻率最高,美國(guó)年新增病例7,155例。結(jié)合HLA-A02:01(人群頻率35.48%)和HLA-A24:02(18.82%),理論可覆蓋3,885例患者。
新抗原肽的鑒定與定量
通過(guò)免疫肽組學(xué)在單等位基因B721.221細(xì)胞中鑒定出HLA-A02:01結(jié)合的10肽(YLDSGIHFGA)和HLA-A24:02結(jié)合的9肽(SYLDSGIHF)。靶向質(zhì)譜顯示Mel888和Hutu80細(xì)胞表面分別呈現(xiàn)101和16個(gè)(HLA-A02:01)以及17和20個(gè)(HLA-A24:02)新抗原肽復(fù)合物,野生型肽幾乎未檢測(cè)到。新抗原肽-MHC復(fù)合物半衰期顯著長(zhǎng)于野生型(HLA-A*02:01:7.3小時(shí) vs 4.1小時(shí))。
TCR篩選與功能驗(yàn)證
從16名健康供體篩選獲得4個(gè)TCR(3個(gè)HLA-A02:01限制性,1個(gè)HLA-A24:02限制性)。TCRA2-2對(duì)肽的敏感性達(dá)499 pM,優(yōu)于臨床級(jí)TCR1G4(24.6 nM)。在重復(fù)殺傷實(shí)驗(yàn)中,TCRA2-2能持續(xù)清除Hutu80A2細(xì)胞,而TCRA24對(duì)Mel888A24的EC50為227 pM。
體內(nèi)治療效果
NXG小鼠模型中,TCRA2-2治療組8天內(nèi)全部清除Mel888A24+A2黑色素瘤(n=7),隨訪(fǎng)115天僅1例復(fù)發(fā);子宮內(nèi)膜癌PDX模型(n=7)中6例達(dá)到完全緩解。值得注意的是,復(fù)發(fā)腫瘤出現(xiàn)HLA-A02:01丟失但保留HLA-A24:02表達(dá),提示免疫編輯機(jī)制差異。
臨床轉(zhuǎn)化潛力
與靶向KRASG12V(年適用16,593例)和TP53R175H(11,638例)相比,CTNNB1S37F適用人群規(guī)模較小,但針對(duì)目前缺乏有效靶向治療的Wnt/β-catenin通路。通過(guò)DRUP類(lèi)試驗(yàn)和HLA分型技術(shù),可篩選適合接受該療法的患者。
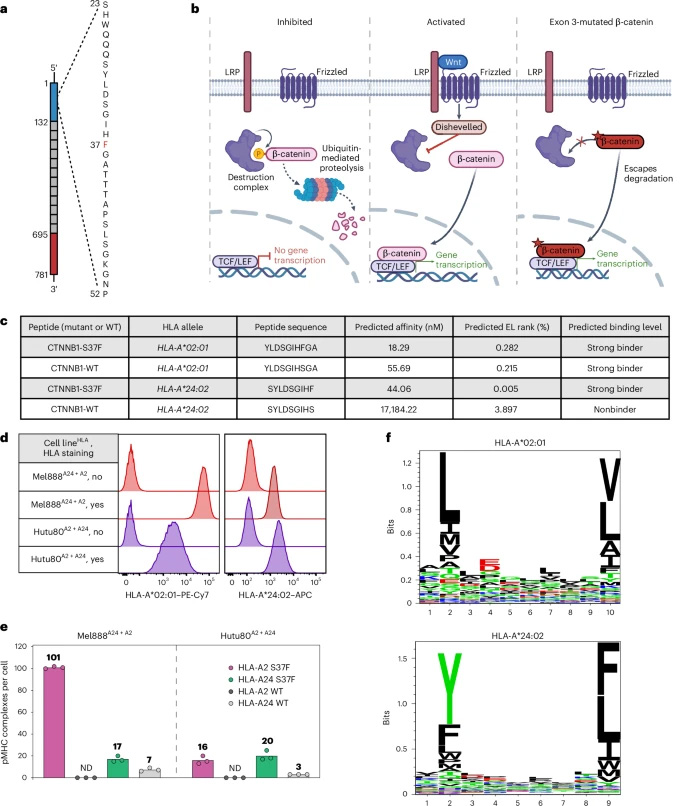
圖2 HLA-A2和HLA-A24分子呈遞的CTNNB1-S37F突變肽段的鑒定與定量分析
討論
該研究突破性地解決了β-catenin靶向治療的兩大難題:通過(guò)MS直接證實(shí)突變肽的遞呈,并利用健康供體TCR庫(kù)克服腫瘤誘導(dǎo)的免疫耐受。雖然突變/HLA組合頻率較低,但針對(duì)驅(qū)動(dòng)突變的特點(diǎn)(如腫瘤早期出現(xiàn)、轉(zhuǎn)移灶保守表達(dá))使其成為聯(lián)合治療的理想靶點(diǎn)。研究為開(kāi)發(fā)靶向其他"不可成藥"癌基因的免疫療法提供了范式。
參考資料
[1] TCR-engineered T cells targeting a shared β-catenin mutation eradicate solid tumors
摘要:研究首次證實(shí)靶向CTNNB1S37F驅(qū)動(dòng)突變的TCR-T細(xì)胞能有效清除表達(dá)HLA-A02:01/HLA-A24:02的實(shí)體瘤。
HLA結(jié)合的復(fù)發(fā)驅(qū)動(dòng)突變肽段是T細(xì)胞免疫治療的潛在靶點(diǎn)。研究發(fā)現(xiàn)CTNNB1S37F突變產(chǎn)生的兩種新抗原肽可被HLA-A02:01和HLA-A24:02遞呈,該突變導(dǎo)致β-catenin功能增強(qiáng),美國(guó)每年新增病例超7,000例。從健康供體幼稚T細(xì)胞中分離出特異性TCR,轉(zhuǎn)導(dǎo)的T細(xì)胞在體外能有效殺傷CTNNB1S37F+細(xì)胞系和患者來(lái)源類(lèi)器官,并在黑色素瘤細(xì)胞系和小鼠子宮內(nèi)膜腺癌PDX模型中清除已形成的腫瘤。

圖1 靶向共享性β-連環(huán)蛋白突變的TCR工程化T細(xì)胞清除實(shí)體瘤
突變癌癥的流行率和發(fā)病率
分析MSK-MET研究25,775例樣本顯示,子宮內(nèi)膜癌(3.35%)、宮頸癌(2.91%)和小腸癌(1.06%)中CTNNB1S37F突變頻率最高,美國(guó)年新增病例7,155例。結(jié)合HLA-A02:01(人群頻率35.48%)和HLA-A24:02(18.82%),理論可覆蓋3,885例患者。
新抗原肽的鑒定與定量
通過(guò)免疫肽組學(xué)在單等位基因B721.221細(xì)胞中鑒定出HLA-A02:01結(jié)合的10肽(YLDSGIHFGA)和HLA-A24:02結(jié)合的9肽(SYLDSGIHF)。靶向質(zhì)譜顯示Mel888和Hutu80細(xì)胞表面分別呈現(xiàn)101和16個(gè)(HLA-A02:01)以及17和20個(gè)(HLA-A24:02)新抗原肽復(fù)合物,野生型肽幾乎未檢測(cè)到。新抗原肽-MHC復(fù)合物半衰期顯著長(zhǎng)于野生型(HLA-A*02:01:7.3小時(shí) vs 4.1小時(shí))。
TCR篩選與功能驗(yàn)證
從16名健康供體篩選獲得4個(gè)TCR(3個(gè)HLA-A02:01限制性,1個(gè)HLA-A24:02限制性)。TCRA2-2對(duì)肽的敏感性達(dá)499 pM,優(yōu)于臨床級(jí)TCR1G4(24.6 nM)。在重復(fù)殺傷實(shí)驗(yàn)中,TCRA2-2能持續(xù)清除Hutu80A2細(xì)胞,而TCRA24對(duì)Mel888A24的EC50為227 pM。
體內(nèi)治療效果
NXG小鼠模型中,TCRA2-2治療組8天內(nèi)全部清除Mel888A24+A2黑色素瘤(n=7),隨訪(fǎng)115天僅1例復(fù)發(fā);子宮內(nèi)膜癌PDX模型(n=7)中6例達(dá)到完全緩解。值得注意的是,復(fù)發(fā)腫瘤出現(xiàn)HLA-A02:01丟失但保留HLA-A24:02表達(dá),提示免疫編輯機(jī)制差異。
臨床轉(zhuǎn)化潛力
與靶向KRASG12V(年適用16,593例)和TP53R175H(11,638例)相比,CTNNB1S37F適用人群規(guī)模較小,但針對(duì)目前缺乏有效靶向治療的Wnt/β-catenin通路。通過(guò)DRUP類(lèi)試驗(yàn)和HLA分型技術(shù),可篩選適合接受該療法的患者。

圖2 HLA-A2和HLA-A24分子呈遞的CTNNB1-S37F突變肽段的鑒定與定量分析
討論
該研究突破性地解決了β-catenin靶向治療的兩大難題:通過(guò)MS直接證實(shí)突變肽的遞呈,并利用健康供體TCR庫(kù)克服腫瘤誘導(dǎo)的免疫耐受。雖然突變/HLA組合頻率較低,但針對(duì)驅(qū)動(dòng)突變的特點(diǎn)(如腫瘤早期出現(xiàn)、轉(zhuǎn)移灶保守表達(dá))使其成為聯(lián)合治療的理想靶點(diǎn)。研究為開(kāi)發(fā)靶向其他"不可成藥"癌基因的免疫療法提供了范式。
參考資料
[1] TCR-engineered T cells targeting a shared β-catenin mutation eradicate solid tumors



