摘要:研究人員開(kāi)展了一項(xiàng)評(píng)估sac-TMT(靶向TROP-2的ADC藥物)聯(lián)合抗PD-L1單抗tagitanlimab一線治療的II期臨床研究(OptiTROP-Lung01)。
在腫瘤治療領(lǐng)域迎來(lái)重要突破!最新發(fā)表在權(quán)威期刊的研究揭示了靶向滋養(yǎng)層細(xì)胞表面抗原2(TROP-2)的抗體偶聯(lián)藥物(ADC)sacituzumab tirumotecan(sac-TMT/MK-2870/SKB264)與程序性死亡配體1(PD-L1)抑制劑tagitanlimab(KL-A167)的強(qiáng)強(qiáng)聯(lián)合。這項(xiàng)代號(hào)為OptiTROP-Lung01的多中心II期臨床試驗(yàn),專門(mén)針對(duì)無(wú)可用藥基因突變的晚期非小細(xì)胞肺癌患者設(shè)計(jì)了兩套創(chuàng)新給藥方案。

圖1 一線戈沙妥珠單抗聯(lián)合泰吉坦利單抗治療晚期非小細(xì)胞肺癌:一項(xiàng)II期臨床試驗(yàn)
研究團(tuán)隊(duì)采用非隨機(jī)分組設(shè)計(jì),將患者分配至不同給藥周期組:1A組每3周接受5 mg/kg sac-TMT聯(lián)合1200 mg tagitanlimab;1B組則采用更密集的每2周5 mg/kg sac-TMT聯(lián)合900 mg tagitanlimab給藥方案。令人振奮的是,在19.3個(gè)月和13.0個(gè)月的中位隨訪期內(nèi),兩組分別斬獲40.0%和66.7%的客觀緩解率,疾病控制率更是高達(dá)85.0%和92.1%。
安全性數(shù)據(jù)同樣亮眼,主要3級(jí)及以上治療相關(guān)不良事件為中性粒細(xì)胞減少(30.0%/34.9%)、白細(xì)胞減少(5.0%/19.0%)和貧血(5.0%/19.0%),未出現(xiàn)治療相關(guān)死亡病例。特別值得注意的是,1B組的中位無(wú)進(jìn)展生存期(PFS)尚未達(dá)到,展現(xiàn)出持久的疾病控制潛力。
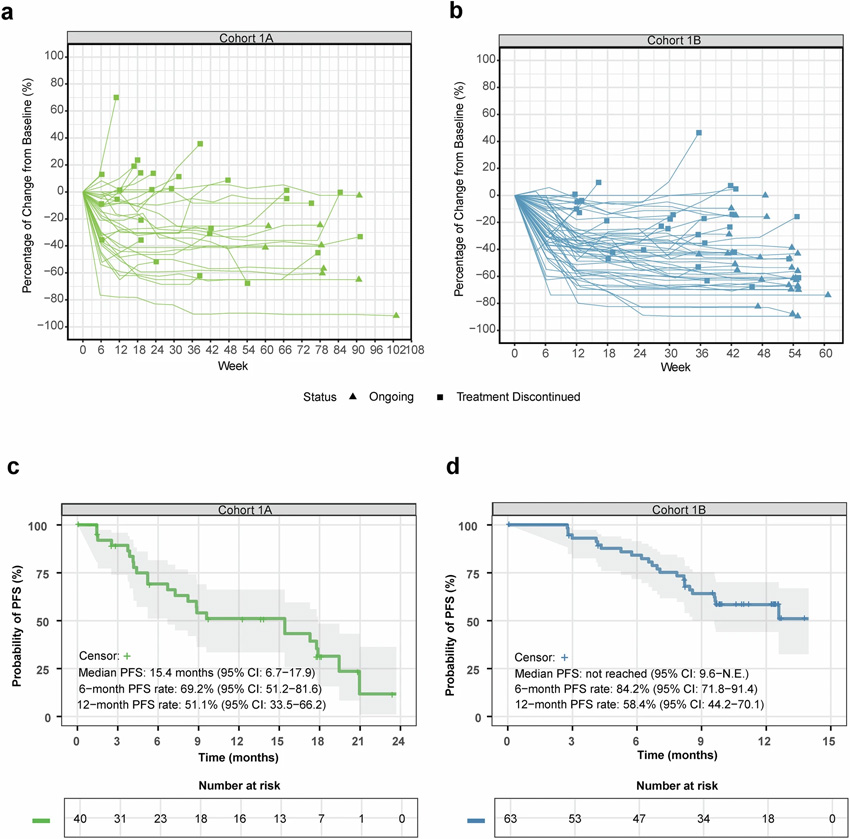
圖2 全分析集人群的療效
這項(xiàng)研究為晚期非小細(xì)胞肺癌的一線治療提供了全新選擇,證實(shí)了靶向TROP-2的ADC與免疫檢查點(diǎn)抑制劑聯(lián)合治療的協(xié)同效應(yīng)。其創(chuàng)新的雙周期給藥方案設(shè)計(jì),更為個(gè)體化治療提供了重要參考。該臨床試驗(yàn)已在ClinicalTrials.gov注冊(cè)(NCT05351788),后續(xù)結(jié)果值得期待。
參考資料
[1] First-line sacituzumab tirumotecan with tagitanlimab in advanced non-small-cell lung cancer: a phase 2 trial
摘要:研究人員開(kāi)展了一項(xiàng)評(píng)估sac-TMT(靶向TROP-2的ADC藥物)聯(lián)合抗PD-L1單抗tagitanlimab一線治療的II期臨床研究(OptiTROP-Lung01)。
在腫瘤治療領(lǐng)域迎來(lái)重要突破!最新發(fā)表在權(quán)威期刊的研究揭示了靶向滋養(yǎng)層細(xì)胞表面抗原2(TROP-2)的抗體偶聯(lián)藥物(ADC)sacituzumab tirumotecan(sac-TMT/MK-2870/SKB264)與程序性死亡配體1(PD-L1)抑制劑tagitanlimab(KL-A167)的強(qiáng)強(qiáng)聯(lián)合。這項(xiàng)代號(hào)為OptiTROP-Lung01的多中心II期臨床試驗(yàn),專門(mén)針對(duì)無(wú)可用藥基因突變的晚期非小細(xì)胞肺癌患者設(shè)計(jì)了兩套創(chuàng)新給藥方案。

圖1 一線戈沙妥珠單抗聯(lián)合泰吉坦利單抗治療晚期非小細(xì)胞肺癌:一項(xiàng)II期臨床試驗(yàn)
研究團(tuán)隊(duì)采用非隨機(jī)分組設(shè)計(jì),將患者分配至不同給藥周期組:1A組每3周接受5 mg/kg sac-TMT聯(lián)合1200 mg tagitanlimab;1B組則采用更密集的每2周5 mg/kg sac-TMT聯(lián)合900 mg tagitanlimab給藥方案。令人振奮的是,在19.3個(gè)月和13.0個(gè)月的中位隨訪期內(nèi),兩組分別斬獲40.0%和66.7%的客觀緩解率,疾病控制率更是高達(dá)85.0%和92.1%。
安全性數(shù)據(jù)同樣亮眼,主要3級(jí)及以上治療相關(guān)不良事件為中性粒細(xì)胞減少(30.0%/34.9%)、白細(xì)胞減少(5.0%/19.0%)和貧血(5.0%/19.0%),未出現(xiàn)治療相關(guān)死亡病例。特別值得注意的是,1B組的中位無(wú)進(jìn)展生存期(PFS)尚未達(dá)到,展現(xiàn)出持久的疾病控制潛力。

圖2 全分析集人群的療效
這項(xiàng)研究為晚期非小細(xì)胞肺癌的一線治療提供了全新選擇,證實(shí)了靶向TROP-2的ADC與免疫檢查點(diǎn)抑制劑聯(lián)合治療的協(xié)同效應(yīng)。其創(chuàng)新的雙周期給藥方案設(shè)計(jì),更為個(gè)體化治療提供了重要參考。該臨床試驗(yàn)已在ClinicalTrials.gov注冊(cè)(NCT05351788),后續(xù)結(jié)果值得期待。
參考資料
[1] First-line sacituzumab tirumotecan with tagitanlimab in advanced non-small-cell lung cancer: a phase 2 trial



