摘要:研究建立了首個(gè)能完整模擬從初始細(xì)胞命運(yùn)決定到器官發(fā)生階段(E8.5-E8.75)的小鼠胚胎模型(iEFC-EM)。
胚胎發(fā)育研究一直是生命科學(xué)領(lǐng)域的重大課題,但現(xiàn)有胚胎模型存在效率低、發(fā)育階段有限、保真度不高等瓶頸問題。傳統(tǒng)方法需要混合多種干細(xì)胞或使用轉(zhuǎn)基因操作,不僅過程復(fù)雜,且難以真實(shí)模擬自然胚胎發(fā)育過程。特別是對(duì)于器官發(fā)生這一關(guān)鍵發(fā)育階段,現(xiàn)有模型更是難以完整重現(xiàn)。這些局限嚴(yán)重制約了發(fā)育生物學(xué)研究和再生醫(yī)學(xué)應(yīng)用。
廣州國家實(shí)驗(yàn)室的研究人員另辟蹊徑,開發(fā)了一種全新的研究策略。他們通過精心設(shè)計(jì)的小分子化合物組合,成功將小鼠胚胎干細(xì)胞(ESCs)直接重編程為具有多能性的8-16細(xì)胞樣胚胎祖細(xì)胞(iEFCs)。這些誘導(dǎo)獲得的胚胎祖細(xì)胞展現(xiàn)出驚人的發(fā)育潛力,能夠自主形成包含所有囊胚譜系的胚胎模型(iEFC-EM),并首次在體外完整重現(xiàn)了從初始細(xì)胞命運(yùn)決定到器官發(fā)生的全過程。這項(xiàng)突破性研究成果發(fā)表在頂級(jí)期刊《Cell》上。

圖1 在化學(xué)誘導(dǎo)胚胎祖細(xì)胞支持下實(shí)現(xiàn)的小鼠胚胎發(fā)生至器官發(fā)生全過程模型
研究人員運(yùn)用了多項(xiàng)關(guān)鍵技術(shù):通過小分子化合物篩選建立高效誘導(dǎo)方案;采用單細(xì)胞RNA測序(scRNA-seq)分析細(xì)胞發(fā)育軌跡;利用轉(zhuǎn)座酶可及染色質(zhì)測序(ATAC-seq)解析表觀遺傳調(diào)控機(jī)制;建立優(yōu)化的胚胎模型培養(yǎng)體系;通過免疫熒光染色和三維成像技術(shù)驗(yàn)證模型發(fā)育特征。特別值得一提的是,研究還構(gòu)建了從E1.5到E6.5的小鼠自然胚胎單細(xì)胞轉(zhuǎn)錄組參考數(shù)據(jù)集,為模型驗(yàn)證提供了重要基準(zhǔn)。
研究結(jié)果部分,文章通過系列實(shí)驗(yàn)系統(tǒng)驗(yàn)證了iEFC-EM模型的發(fā)育保真度:
"Screen identifies small molecules that reprogram ESCs into EFCs"顯示,優(yōu)化的K4處理方案(含CHIR99021、E616452和AM580)可高效誘導(dǎo)ESCs共表達(dá)OCT4、GATA6和CDX2,形成分子特征類似8-16細(xì)胞期胚胎的iEFCs。單細(xì)胞分析證實(shí)這些細(xì)胞與自然胚胎的轉(zhuǎn)錄組特征高度匹配。
"iEFCs segregate all blastocyst lineages both in vivo and in vitro"證實(shí),iEFCs在體內(nèi)外實(shí)驗(yàn)中均能分化為所有囊胚譜系。嵌合實(shí)驗(yàn)顯示iEFCs可貢獻(xiàn)到E6.5胚胎的所有胚層,而單細(xì)胞測序進(jìn)一步驗(yàn)證了其在胚胎和胚外組織中的均衡分布。
"iEFCs specify all blastocyst fates faithfully and rapidly"發(fā)現(xiàn),經(jīng)過36小時(shí)的定向誘導(dǎo),iEFCs可快速分化為上胚層(EPI)、原始內(nèi)胚層(PrE)和滋養(yǎng)外胚層(TE),并形成具有極性TE和壁TE特征的復(fù)雜結(jié)構(gòu)。
"iEFC-derived embryo model recapitulates embryo development faithfully"展示,iEFC-EM模型在8天內(nèi)依次重現(xiàn)了譜系特化、腔體形成、對(duì)稱性打破、原腸形成等關(guān)鍵發(fā)育事件,最終形成具有14對(duì)體節(jié)、跳動(dòng)心管、神經(jīng)褶等器官發(fā)生期特征的胚胎樣結(jié)構(gòu)。
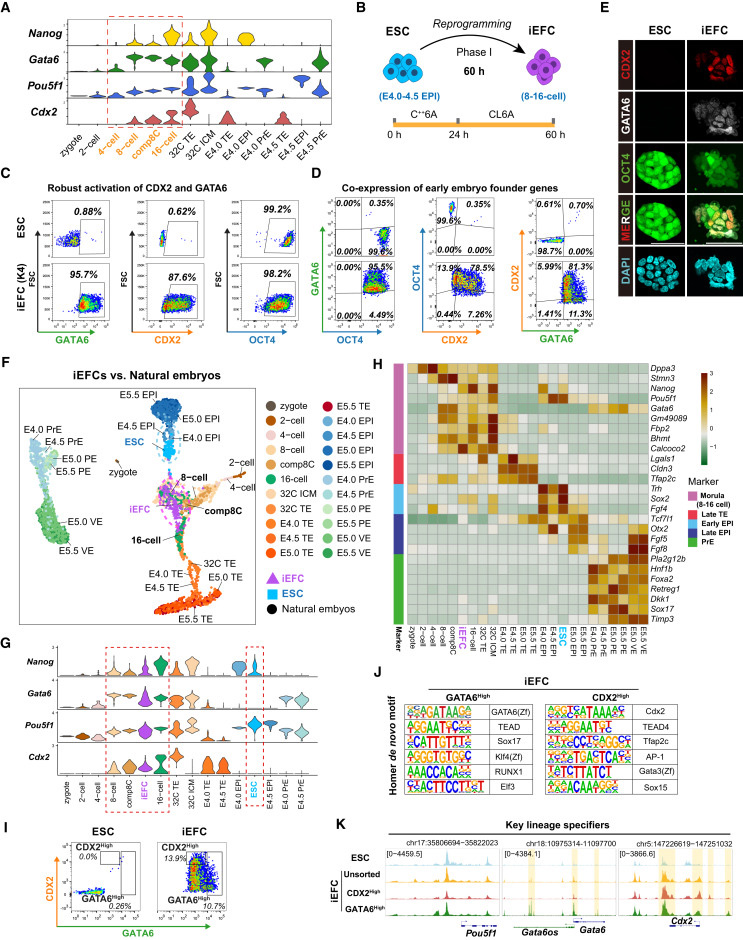
圖2 候選分子篩選鑒定出可將胚胎干細(xì)胞重編程為類胚胎祖細(xì)胞的小分子化合物
"Day-6 iEFC-EMs display high-fidelity E7.5 molecular signature"通過單細(xì)胞轉(zhuǎn)錄組分析證實(shí),第6天的iEFC-EM與E7.5自然胚胎在分子特征上高度相似,包含24種細(xì)胞類型,重現(xiàn)了原條形成、上皮-間質(zhì)轉(zhuǎn)化(EMT)等原腸胚形成過程。
"iEFC-EMs display advanced trophoblast lineage development"揭示,模型中的胚外組織發(fā)育同樣高度保真,不僅形成復(fù)雜的滋養(yǎng)層亞型,還能誘導(dǎo)子宮蛻膜化,提示其可能分泌未知的母體信號(hào)分子。
"iEFC-EMs reach organogenesis efficiently and with high fidelity"顯示,第8天的模型形成了包括前/中/后腦、心管、視泡、尾芽等器官原基,單細(xì)胞測序鑒定出20種胚胎和7種胚外細(xì)胞類型,其轉(zhuǎn)錄特征與E8.5自然胚胎高度一致。
"Neurulation and surface ectoderm development"證實(shí),iEFC-EM的神經(jīng)外胚層發(fā)育遵循自然胚胎的時(shí)空模式,正確表達(dá)了OTX2(前腦和中腦)、PAX6(前腦和后腦)等區(qū)域特異性標(biāo)記。
"Somitogenesis, cardiogenesis and mesodermal development"顯示,模型中的體節(jié)發(fā)生、心臟發(fā)育等中胚層衍生物與自然胚胎相似,心管呈現(xiàn)正確的環(huán)化形態(tài)和收縮功能。
"Endoderm development and PGC progression"發(fā)現(xiàn),模型不僅形成明確的前腸和后腸結(jié)構(gòu),還產(chǎn)生了正在遷移的原始生殖細(xì)胞(PGCs),其分子特征與體內(nèi)發(fā)育的PGCs高度一致。
這項(xiàng)研究在多個(gè)方面具有重要意義:首先,iEFC-EM模型首次實(shí)現(xiàn)了從干細(xì)胞到器官發(fā)生階段的完整胚胎發(fā)育過程模擬,為研究早期發(fā)育機(jī)制提供了全新工具;其次,完全化學(xué)小分子誘導(dǎo)的策略避免了轉(zhuǎn)基因操作,更具應(yīng)用潛力;再者,模型的高效率(54.2%達(dá)到器官發(fā)生階段)和可擴(kuò)展性使其適合大規(guī)模篩選應(yīng)用。特別值得注意的是,研究揭示了胚胎可能通過特定信號(hào)分子主動(dòng)參與母體蛻膜化過程,這一發(fā)現(xiàn)為理解胚胎-母體對(duì)話提供了新線索。
盡管iEFC-EM模型在發(fā)育保真度上取得重大突破,作者也指出了當(dāng)前局限:模型缺乏與子宮壁接觸的壁TE結(jié)構(gòu),這可能是其難以突破E8.5發(fā)育階段的關(guān)鍵因素。未來研究需要進(jìn)一步優(yōu)化培養(yǎng)條件,解析維持后期發(fā)育的母體信號(hào),以充分發(fā)揮這一系統(tǒng)的應(yīng)用潛力。這項(xiàng)研究不僅為發(fā)育生物學(xué)研究樹立了新標(biāo)桿,也為器官再生、疾病建模和生殖醫(yī)學(xué)等領(lǐng)域帶來了新的可能性。
參考資料
[1] A complete model of mouse embryogenesis through organogenesis enabled by chemically induced embryo founder cells
摘要:研究建立了首個(gè)能完整模擬從初始細(xì)胞命運(yùn)決定到器官發(fā)生階段(E8.5-E8.75)的小鼠胚胎模型(iEFC-EM)。
胚胎發(fā)育研究一直是生命科學(xué)領(lǐng)域的重大課題,但現(xiàn)有胚胎模型存在效率低、發(fā)育階段有限、保真度不高等瓶頸問題。傳統(tǒng)方法需要混合多種干細(xì)胞或使用轉(zhuǎn)基因操作,不僅過程復(fù)雜,且難以真實(shí)模擬自然胚胎發(fā)育過程。特別是對(duì)于器官發(fā)生這一關(guān)鍵發(fā)育階段,現(xiàn)有模型更是難以完整重現(xiàn)。這些局限嚴(yán)重制約了發(fā)育生物學(xué)研究和再生醫(yī)學(xué)應(yīng)用。
廣州國家實(shí)驗(yàn)室的研究人員另辟蹊徑,開發(fā)了一種全新的研究策略。他們通過精心設(shè)計(jì)的小分子化合物組合,成功將小鼠胚胎干細(xì)胞(ESCs)直接重編程為具有多能性的8-16細(xì)胞樣胚胎祖細(xì)胞(iEFCs)。這些誘導(dǎo)獲得的胚胎祖細(xì)胞展現(xiàn)出驚人的發(fā)育潛力,能夠自主形成包含所有囊胚譜系的胚胎模型(iEFC-EM),并首次在體外完整重現(xiàn)了從初始細(xì)胞命運(yùn)決定到器官發(fā)生的全過程。這項(xiàng)突破性研究成果發(fā)表在頂級(jí)期刊《Cell》上。

圖1 在化學(xué)誘導(dǎo)胚胎祖細(xì)胞支持下實(shí)現(xiàn)的小鼠胚胎發(fā)生至器官發(fā)生全過程模型
研究人員運(yùn)用了多項(xiàng)關(guān)鍵技術(shù):通過小分子化合物篩選建立高效誘導(dǎo)方案;采用單細(xì)胞RNA測序(scRNA-seq)分析細(xì)胞發(fā)育軌跡;利用轉(zhuǎn)座酶可及染色質(zhì)測序(ATAC-seq)解析表觀遺傳調(diào)控機(jī)制;建立優(yōu)化的胚胎模型培養(yǎng)體系;通過免疫熒光染色和三維成像技術(shù)驗(yàn)證模型發(fā)育特征。特別值得一提的是,研究還構(gòu)建了從E1.5到E6.5的小鼠自然胚胎單細(xì)胞轉(zhuǎn)錄組參考數(shù)據(jù)集,為模型驗(yàn)證提供了重要基準(zhǔn)。
研究結(jié)果部分,文章通過系列實(shí)驗(yàn)系統(tǒng)驗(yàn)證了iEFC-EM模型的發(fā)育保真度:
"Screen identifies small molecules that reprogram ESCs into EFCs"顯示,優(yōu)化的K4處理方案(含CHIR99021、E616452和AM580)可高效誘導(dǎo)ESCs共表達(dá)OCT4、GATA6和CDX2,形成分子特征類似8-16細(xì)胞期胚胎的iEFCs。單細(xì)胞分析證實(shí)這些細(xì)胞與自然胚胎的轉(zhuǎn)錄組特征高度匹配。
"iEFCs segregate all blastocyst lineages both in vivo and in vitro"證實(shí),iEFCs在體內(nèi)外實(shí)驗(yàn)中均能分化為所有囊胚譜系。嵌合實(shí)驗(yàn)顯示iEFCs可貢獻(xiàn)到E6.5胚胎的所有胚層,而單細(xì)胞測序進(jìn)一步驗(yàn)證了其在胚胎和胚外組織中的均衡分布。
"iEFCs specify all blastocyst fates faithfully and rapidly"發(fā)現(xiàn),經(jīng)過36小時(shí)的定向誘導(dǎo),iEFCs可快速分化為上胚層(EPI)、原始內(nèi)胚層(PrE)和滋養(yǎng)外胚層(TE),并形成具有極性TE和壁TE特征的復(fù)雜結(jié)構(gòu)。
"iEFC-derived embryo model recapitulates embryo development faithfully"展示,iEFC-EM模型在8天內(nèi)依次重現(xiàn)了譜系特化、腔體形成、對(duì)稱性打破、原腸形成等關(guān)鍵發(fā)育事件,最終形成具有14對(duì)體節(jié)、跳動(dòng)心管、神經(jīng)褶等器官發(fā)生期特征的胚胎樣結(jié)構(gòu)。

圖2 候選分子篩選鑒定出可將胚胎干細(xì)胞重編程為類胚胎祖細(xì)胞的小分子化合物
"Day-6 iEFC-EMs display high-fidelity E7.5 molecular signature"通過單細(xì)胞轉(zhuǎn)錄組分析證實(shí),第6天的iEFC-EM與E7.5自然胚胎在分子特征上高度相似,包含24種細(xì)胞類型,重現(xiàn)了原條形成、上皮-間質(zhì)轉(zhuǎn)化(EMT)等原腸胚形成過程。
"iEFC-EMs display advanced trophoblast lineage development"揭示,模型中的胚外組織發(fā)育同樣高度保真,不僅形成復(fù)雜的滋養(yǎng)層亞型,還能誘導(dǎo)子宮蛻膜化,提示其可能分泌未知的母體信號(hào)分子。
"iEFC-EMs reach organogenesis efficiently and with high fidelity"顯示,第8天的模型形成了包括前/中/后腦、心管、視泡、尾芽等器官原基,單細(xì)胞測序鑒定出20種胚胎和7種胚外細(xì)胞類型,其轉(zhuǎn)錄特征與E8.5自然胚胎高度一致。
"Neurulation and surface ectoderm development"證實(shí),iEFC-EM的神經(jīng)外胚層發(fā)育遵循自然胚胎的時(shí)空模式,正確表達(dá)了OTX2(前腦和中腦)、PAX6(前腦和后腦)等區(qū)域特異性標(biāo)記。
"Somitogenesis, cardiogenesis and mesodermal development"顯示,模型中的體節(jié)發(fā)生、心臟發(fā)育等中胚層衍生物與自然胚胎相似,心管呈現(xiàn)正確的環(huán)化形態(tài)和收縮功能。
"Endoderm development and PGC progression"發(fā)現(xiàn),模型不僅形成明確的前腸和后腸結(jié)構(gòu),還產(chǎn)生了正在遷移的原始生殖細(xì)胞(PGCs),其分子特征與體內(nèi)發(fā)育的PGCs高度一致。
這項(xiàng)研究在多個(gè)方面具有重要意義:首先,iEFC-EM模型首次實(shí)現(xiàn)了從干細(xì)胞到器官發(fā)生階段的完整胚胎發(fā)育過程模擬,為研究早期發(fā)育機(jī)制提供了全新工具;其次,完全化學(xué)小分子誘導(dǎo)的策略避免了轉(zhuǎn)基因操作,更具應(yīng)用潛力;再者,模型的高效率(54.2%達(dá)到器官發(fā)生階段)和可擴(kuò)展性使其適合大規(guī)模篩選應(yīng)用。特別值得注意的是,研究揭示了胚胎可能通過特定信號(hào)分子主動(dòng)參與母體蛻膜化過程,這一發(fā)現(xiàn)為理解胚胎-母體對(duì)話提供了新線索。
盡管iEFC-EM模型在發(fā)育保真度上取得重大突破,作者也指出了當(dāng)前局限:模型缺乏與子宮壁接觸的壁TE結(jié)構(gòu),這可能是其難以突破E8.5發(fā)育階段的關(guān)鍵因素。未來研究需要進(jìn)一步優(yōu)化培養(yǎng)條件,解析維持后期發(fā)育的母體信號(hào),以充分發(fā)揮這一系統(tǒng)的應(yīng)用潛力。這項(xiàng)研究不僅為發(fā)育生物學(xué)研究樹立了新標(biāo)桿,也為器官再生、疾病建模和生殖醫(yī)學(xué)等領(lǐng)域帶來了新的可能性。
參考資料
[1] A complete model of mouse embryogenesis through organogenesis enabled by chemically induced embryo founder cells



