摘要:研究者發(fā)現(xiàn)circRNA BISC通過特異性靶向RNA結合蛋白IGF2BP2,抑制c-MYC mRNA翻譯從而逆轉(zhuǎn)耐藥
在腫瘤治療領域,BET蛋白家族作為識別乙?;M蛋白的表觀遺傳"閱讀器",通過調(diào)控c-MYC等癌基因表達成為重要靶點。然而BET抑制劑(BETi)在臨床應用中面臨嚴峻挑戰(zhàn)——約50%實體瘤試驗因快速出現(xiàn)的獲得性耐藥而終止。這種耐藥性在c-MYC高度依賴的三陰性乳腺癌(TNBC)中尤為突出,傳統(tǒng)策略如聯(lián)合用藥往往伴隨毒性增加,迫切需要揭示耐藥機制并開發(fā)精準干預手段。
針對這一關鍵科學問題,研究人員通過系統(tǒng)分析發(fā)現(xiàn),耐藥TNBC細胞中circRNA BISC表達顯著降低,而RNA結合蛋白IGF2BP2異常激活。進一步研究揭示,BISC含有獨特的"CAC-|9-12|-XGGX"基序,能特異性結合IGF2BP2的KH3/KH4結構域,從而競爭性阻斷IGF2BP2與c-MYC mRNA的相互作用。

圖1 環(huán)狀RNA適配體靶向IGF2BP2以克服獲得性BETi耐藥性
這種circRNA-RBP互作模式突破了傳統(tǒng)表觀遺傳藥物的作用框架,為克服耐藥性提供了新視角。
研究團隊采用多組學聯(lián)用策略:首先通過全轉(zhuǎn)錄組測序鑒定耐藥相關circRNA表達譜;建立CRISPR-Cas13b高通量篩選平臺驗證功能circRNA;結合RIP-seq(RNA免疫沉淀測序)分析IGF2BP2結合RNA動態(tài)變化;運用生物信息學預測RNA-蛋白互作基序;最后在PDX模型中評估體外轉(zhuǎn)錄環(huán)化BISC的治療效果。樣本來源于臨床耐藥TNBC患者源性異種移植模型。
主要研究發(fā)現(xiàn)包括:
耐藥機制解析:證實BETi長期暴露導致BISC下調(diào),釋放的IGF2BP2增強c-MYC mRNA翻譯效率,獨立于β-catenin/GLI2/MED1轉(zhuǎn)錄調(diào)控通路。
分子互作驗證:結構生物學分析揭示BISC通過KH3/KH4結構域選擇性抑制IGF2BP2,與同源蛋白IGF2BP1/3無交叉作用。
治療策略開發(fā):靜脈注射的環(huán)化BISC在腫瘤組織特異性富集,與OTX015聯(lián)用顯著抑制耐藥TNBC生長,且通過肝腎快速清除降低系統(tǒng)毒性。
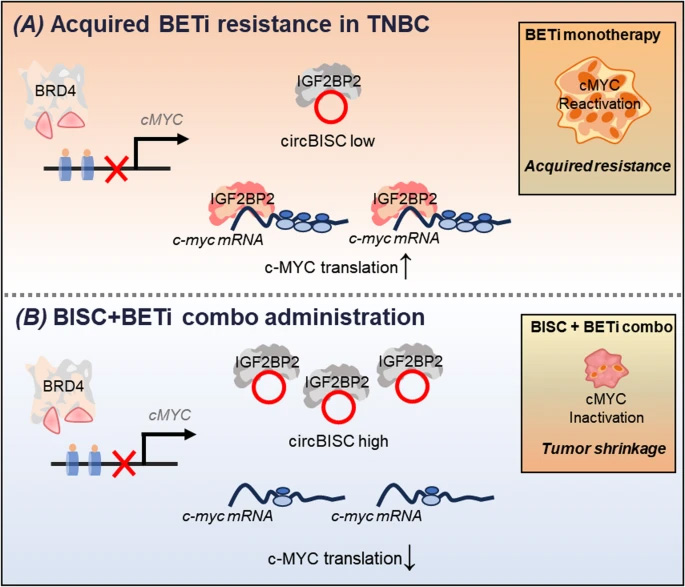
圖2 三陰性乳腺癌中獲得性BETi耐藥性的分子機制
這項研究的突破性意義體現(xiàn)在三個維度:科學層面,首次闡明circRNA通過翻譯調(diào)控參與表觀遺傳藥物耐藥的新機制;技術層面,建立"目標導向"的circRNA篩選范式,突破傳統(tǒng)差異表達分析的局限性;臨床層面,開發(fā)出具有明確作用靶點的circRNA療法,其模塊化設計可拓展至其他"不可成藥"RBP靶點。該成果為TNBC精準治療提供新工具,同時為circRNA藥物的臨床轉(zhuǎn)化奠定重要基礎。
參考資料
[1] CircRNA aptamer targets IGF2BP2 to overcome acquired BETi resistance
摘要:研究者發(fā)現(xiàn)circRNA BISC通過特異性靶向RNA結合蛋白IGF2BP2,抑制c-MYC mRNA翻譯從而逆轉(zhuǎn)耐藥
在腫瘤治療領域,BET蛋白家族作為識別乙?;M蛋白的表觀遺傳"閱讀器",通過調(diào)控c-MYC等癌基因表達成為重要靶點。然而BET抑制劑(BETi)在臨床應用中面臨嚴峻挑戰(zhàn)——約50%實體瘤試驗因快速出現(xiàn)的獲得性耐藥而終止。這種耐藥性在c-MYC高度依賴的三陰性乳腺癌(TNBC)中尤為突出,傳統(tǒng)策略如聯(lián)合用藥往往伴隨毒性增加,迫切需要揭示耐藥機制并開發(fā)精準干預手段。
針對這一關鍵科學問題,研究人員通過系統(tǒng)分析發(fā)現(xiàn),耐藥TNBC細胞中circRNA BISC表達顯著降低,而RNA結合蛋白IGF2BP2異常激活。進一步研究揭示,BISC含有獨特的"CAC-|9-12|-XGGX"基序,能特異性結合IGF2BP2的KH3/KH4結構域,從而競爭性阻斷IGF2BP2與c-MYC mRNA的相互作用。

圖1 環(huán)狀RNA適配體靶向IGF2BP2以克服獲得性BETi耐藥性
這種circRNA-RBP互作模式突破了傳統(tǒng)表觀遺傳藥物的作用框架,為克服耐藥性提供了新視角。
研究團隊采用多組學聯(lián)用策略:首先通過全轉(zhuǎn)錄組測序鑒定耐藥相關circRNA表達譜;建立CRISPR-Cas13b高通量篩選平臺驗證功能circRNA;結合RIP-seq(RNA免疫沉淀測序)分析IGF2BP2結合RNA動態(tài)變化;運用生物信息學預測RNA-蛋白互作基序;最后在PDX模型中評估體外轉(zhuǎn)錄環(huán)化BISC的治療效果。樣本來源于臨床耐藥TNBC患者源性異種移植模型。
主要研究發(fā)現(xiàn)包括:
耐藥機制解析:證實BETi長期暴露導致BISC下調(diào),釋放的IGF2BP2增強c-MYC mRNA翻譯效率,獨立于β-catenin/GLI2/MED1轉(zhuǎn)錄調(diào)控通路。
分子互作驗證:結構生物學分析揭示BISC通過KH3/KH4結構域選擇性抑制IGF2BP2,與同源蛋白IGF2BP1/3無交叉作用。
治療策略開發(fā):靜脈注射的環(huán)化BISC在腫瘤組織特異性富集,與OTX015聯(lián)用顯著抑制耐藥TNBC生長,且通過肝腎快速清除降低系統(tǒng)毒性。

圖2 三陰性乳腺癌中獲得性BETi耐藥性的分子機制
這項研究的突破性意義體現(xiàn)在三個維度:科學層面,首次闡明circRNA通過翻譯調(diào)控參與表觀遺傳藥物耐藥的新機制;技術層面,建立"目標導向"的circRNA篩選范式,突破傳統(tǒng)差異表達分析的局限性;臨床層面,開發(fā)出具有明確作用靶點的circRNA療法,其模塊化設計可拓展至其他"不可成藥"RBP靶點。該成果為TNBC精準治療提供新工具,同時為circRNA藥物的臨床轉(zhuǎn)化奠定重要基礎。
參考資料
[1] CircRNA aptamer targets IGF2BP2 to overcome acquired BETi resistance



