摘要:首次揭示糖尿病前期微環(huán)境通過上調(diào)載脂蛋白CIII(apoCIII)表達(dá)誘發(fā)胰島炎癥反應(yīng)和β細(xì)胞凋亡的分子機(jī)制。
在全球范圍內(nèi),1型糖尿?。═1D)發(fā)病率呈現(xiàn)令人擔(dān)憂的上升趨勢(shì),且發(fā)病年齡不斷提前。這種自身免疫性疾病的核心特征是胰腺β細(xì)胞的進(jìn)行性破壞,導(dǎo)致胰島素絕對(duì)缺乏。雖然胰島移植被視為潛在治療方案,但移植后的胰島存活率始終不理想——即使采用免疫抑制治療,移植到肝臟門靜脈系統(tǒng)的胰島仍難以長(zhǎng)期存活,患者往往需要多次移植才能維持胰島素分泌功能。這一臨床困境引出了兩個(gè)關(guān)鍵科學(xué)問題:是否存在更優(yōu)化的移植位點(diǎn)?能否通過生物工程手段增強(qiáng)胰島對(duì)免疫攻擊的抵抗力?
來自卡羅林斯卡醫(yī)學(xué)院(Karolinska Institutet)和西華醫(yī)院(West China Hospital)的聯(lián)合研究團(tuán)隊(duì)在《Signal Transduction and Targeted Therapy》發(fā)表了一項(xiàng)突破性研究。研究人員創(chuàng)新性地利用BioBreeding(BB)大鼠模型,通過眼前房移植技術(shù)結(jié)合多模態(tài)成像,首次在活體水平揭示了糖尿病前期微環(huán)境對(duì)胰島功能的決定性影響。研究發(fā)現(xiàn)載脂蛋白CIII(apoCIII)作為關(guān)鍵介質(zhì),通過激活炎癥小體和促炎因子IL-1β,驅(qū)動(dòng)了移植胰島的血管退化和β細(xì)胞凋亡。這一發(fā)現(xiàn)不僅闡明了T1D發(fā)病的微環(huán)境調(diào)控機(jī)制,更為開發(fā)抗炎性工程化胰島提供了明確靶點(diǎn)。

圖1 BioBreading大鼠模型中胰島環(huán)境與1型糖尿病發(fā)生
研究團(tuán)隊(duì)采用了三項(xiàng)關(guān)鍵技術(shù):1)糖尿病易感(DP)和抗性(DR)BB大鼠模型的建立與表征;2)眼前房移植技術(shù)實(shí)現(xiàn)胰島移植后的長(zhǎng)期無創(chuàng)監(jiān)測(cè);3)激光共聚焦顯微成像定量分析胰島血管化和炎癥浸潤。通過交叉移植實(shí)驗(yàn)設(shè)計(jì)(將DP大鼠胰島移植至DR大鼠眼前房,反之亦然),結(jié)合qRT-PCR、免疫熒光和體積定量分析等方法,系統(tǒng)評(píng)估了不同微環(huán)境對(duì)胰島功能的影響。
研究結(jié)果揭示:
1)微環(huán)境決定胰島命運(yùn):盡管移植初期所有胰島均能成功血管化,但處于糖尿病前期環(huán)境的DR胰島在T1D發(fā)病年齡附近出現(xiàn)功能性血管幾乎完全喪失,血管密度較基線下降顯著(p<0.05)。< div="">
圖1 BioBreading大鼠模型中胰島環(huán)境與1型糖尿病發(fā)生
2)apoCIII的核心作用:免疫染色顯示apoCIII在α和β細(xì)胞均有表達(dá),且糖尿病前期胰島中apoCIII陽性細(xì)胞顯著增多(胰腺組織:DP 53.7±8.5% vs DR 75.5±3.4%;眼前房移植胰島:DP 33.6±4.2% vs DR 56.8±3.3%)。這種差異具有統(tǒng)計(jì)學(xué)意義(p<0.05)。< div="">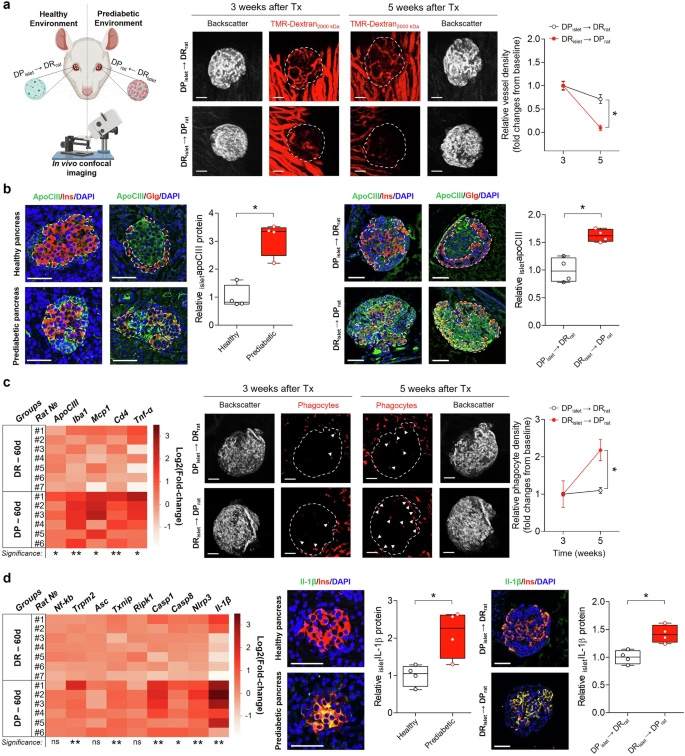
圖2 健康胰島移植至糖尿病前期環(huán)境及反向移植的效應(yīng)
3)炎癥級(jí)聯(lián)反應(yīng):60日齡DP大鼠胰島顯示apoCIII上調(diào)伴隨炎癥標(biāo)志物(Iba1、Mcp1、Cd4、Tnf-α)的顯著增加。炎癥小體相關(guān)基因的激活導(dǎo)致IL-1β水平升高,這一現(xiàn)象在移植至DP環(huán)境的DR胰島中同樣被觀察到。
4)臨床轉(zhuǎn)化價(jià)值:研究證實(shí)降低apoCIII表達(dá)可延緩T1D發(fā)病,提示其作為治療靶點(diǎn)的潛力。團(tuán)隊(duì)計(jì)劃利用CRISPR/Cas9技術(shù)構(gòu)建apoCIII低表達(dá)的人胰島類器官,以驗(yàn)證其在糖尿病環(huán)境中的抵抗力。

圖2 健康胰島移植至糖尿病前期環(huán)境及反向移植的效應(yīng)
這項(xiàng)研究的重要意義在于:首次在活體水平證實(shí)胰島微環(huán)境而非胰島自身特性決定移植結(jié)局;確立apoCIII-炎癥小體軸作為T1D進(jìn)展的關(guān)鍵調(diào)控通路;提出眼前房作為潛在移植位點(diǎn)的臨床價(jià)值。研究由Patricia Recio-López、Per-Olof Berggren等學(xué)者完成,創(chuàng)新性地將基礎(chǔ)研究與臨床轉(zhuǎn)化相結(jié)合,為開發(fā)新一代抗炎性工程化胰島提供了理論依據(jù)和技術(shù)路線。特別值得注意的是,該團(tuán)隊(duì)發(fā)現(xiàn)通過反義寡核苷酸降低apoCIII水平可延遲T1D發(fā)病,這一策略可能改寫當(dāng)前胰島移植的治療范式。
參考資料
[1] Islet environment and development of type 1 diabetes in the biobreeding rat model
摘要:首次揭示糖尿病前期微環(huán)境通過上調(diào)載脂蛋白CIII(apoCIII)表達(dá)誘發(fā)胰島炎癥反應(yīng)和β細(xì)胞凋亡的分子機(jī)制。
在全球范圍內(nèi),1型糖尿病(T1D)發(fā)病率呈現(xiàn)令人擔(dān)憂的上升趨勢(shì),且發(fā)病年齡不斷提前。這種自身免疫性疾病的核心特征是胰腺β細(xì)胞的進(jìn)行性破壞,導(dǎo)致胰島素絕對(duì)缺乏。雖然胰島移植被視為潛在治療方案,但移植后的胰島存活率始終不理想——即使采用免疫抑制治療,移植到肝臟門靜脈系統(tǒng)的胰島仍難以長(zhǎng)期存活,患者往往需要多次移植才能維持胰島素分泌功能。這一臨床困境引出了兩個(gè)關(guān)鍵科學(xué)問題:是否存在更優(yōu)化的移植位點(diǎn)?能否通過生物工程手段增強(qiáng)胰島對(duì)免疫攻擊的抵抗力?
來自卡羅林斯卡醫(yī)學(xué)院(Karolinska Institutet)和西華醫(yī)院(West China Hospital)的聯(lián)合研究團(tuán)隊(duì)在《Signal Transduction and Targeted Therapy》發(fā)表了一項(xiàng)突破性研究。研究人員創(chuàng)新性地利用BioBreeding(BB)大鼠模型,通過眼前房移植技術(shù)結(jié)合多模態(tài)成像,首次在活體水平揭示了糖尿病前期微環(huán)境對(duì)胰島功能的決定性影響。研究發(fā)現(xiàn)載脂蛋白CIII(apoCIII)作為關(guān)鍵介質(zhì),通過激活炎癥小體和促炎因子IL-1β,驅(qū)動(dòng)了移植胰島的血管退化和β細(xì)胞凋亡。這一發(fā)現(xiàn)不僅闡明了T1D發(fā)病的微環(huán)境調(diào)控機(jī)制,更為開發(fā)抗炎性工程化胰島提供了明確靶點(diǎn)。

圖1 BioBreading大鼠模型中胰島環(huán)境與1型糖尿病發(fā)生
研究團(tuán)隊(duì)采用了三項(xiàng)關(guān)鍵技術(shù):1)糖尿病易感(DP)和抗性(DR)BB大鼠模型的建立與表征;2)眼前房移植技術(shù)實(shí)現(xiàn)胰島移植后的長(zhǎng)期無創(chuàng)監(jiān)測(cè);3)激光共聚焦顯微成像定量分析胰島血管化和炎癥浸潤。通過交叉移植實(shí)驗(yàn)設(shè)計(jì)(將DP大鼠胰島移植至DR大鼠眼前房,反之亦然),結(jié)合qRT-PCR、免疫熒光和體積定量分析等方法,系統(tǒng)評(píng)估了不同微環(huán)境對(duì)胰島功能的影響。
研究結(jié)果揭示:
1)微環(huán)境決定胰島命運(yùn):盡管移植初期所有胰島均能成功血管化,但處于糖尿病前期環(huán)境的DR胰島在T1D發(fā)病年齡附近出現(xiàn)功能性血管幾乎完全喪失,血管密度較基線下降顯著(p<0.05)。< div="">
2)apoCIII的核心作用:免疫染色顯示apoCIII在α和β細(xì)胞均有表達(dá),且糖尿病前期胰島中apoCIII陽性細(xì)胞顯著增多(胰腺組織:DP 53.7±8.5% vs DR 75.5±3.4%;眼前房移植胰島:DP 33.6±4.2% vs DR 56.8±3.3%)。這種差異具有統(tǒng)計(jì)學(xué)意義(p<0.05)。< div="">
圖2 健康胰島移植至糖尿病前期環(huán)境及反向移植的效應(yīng)
3)炎癥級(jí)聯(lián)反應(yīng):60日齡DP大鼠胰島顯示apoCIII上調(diào)伴隨炎癥標(biāo)志物(Iba1、Mcp1、Cd4、Tnf-α)的顯著增加。炎癥小體相關(guān)基因的激活導(dǎo)致IL-1β水平升高,這一現(xiàn)象在移植至DP環(huán)境的DR胰島中同樣被觀察到。
4)臨床轉(zhuǎn)化價(jià)值:研究證實(shí)降低apoCIII表達(dá)可延緩T1D發(fā)病,提示其作為治療靶點(diǎn)的潛力。團(tuán)隊(duì)計(jì)劃利用CRISPR/Cas9技術(shù)構(gòu)建apoCIII低表達(dá)的人胰島類器官,以驗(yàn)證其在糖尿病環(huán)境中的抵抗力。

圖2 健康胰島移植至糖尿病前期環(huán)境及反向移植的效應(yīng)
這項(xiàng)研究的重要意義在于:首次在活體水平證實(shí)胰島微環(huán)境而非胰島自身特性決定移植結(jié)局;確立apoCIII-炎癥小體軸作為T1D進(jìn)展的關(guān)鍵調(diào)控通路;提出眼前房作為潛在移植位點(diǎn)的臨床價(jià)值。研究由Patricia Recio-López、Per-Olof Berggren等學(xué)者完成,創(chuàng)新性地將基礎(chǔ)研究與臨床轉(zhuǎn)化相結(jié)合,為開發(fā)新一代抗炎性工程化胰島提供了理論依據(jù)和技術(shù)路線。特別值得注意的是,該團(tuán)隊(duì)發(fā)現(xiàn)通過反義寡核苷酸降低apoCIII水平可延遲T1D發(fā)病,這一策略可能改寫當(dāng)前胰島移植的治療范式。
參考資料
[1] Islet environment and development of type 1 diabetes in the biobreeding rat model



