摘要: 本綜述深入探討了免疫代謝在腫瘤微環(huán)境(TME)中的關(guān)鍵作用。
診斷與治療標(biāo)準(zhǔn)的進(jìn)步顯著提高了惡性腫瘤患者的生存率。然而,尋找有效策略以應(yīng)對(duì)耐藥性或復(fù)發(fā)性晚期腫瘤,仍然是一個(gè)至關(guān)重要且堅(jiān)定不移的目標(biāo)。雙特異性抗體(BsAbs)通過(guò)同時(shí)結(jié)合兩個(gè)不同靶點(diǎn),從而提高了特異性、最大程度減少了脫靶毒性,并能協(xié)同調(diào)節(jié)抗腫瘤免疫和腫瘤微環(huán)境,由此開啟了抗腫瘤治療的新時(shí)代。與兩種單克隆抗體聯(lián)用相比,BsAbs代表了雙特異性的物理整合,展現(xiàn)出更優(yōu)的結(jié)合效力,降低了耐藥風(fēng)險(xiǎn),并實(shí)現(xiàn)了獨(dú)特的生物學(xué)功能,例如橋接腫瘤細(xì)胞和T細(xì)胞以實(shí)現(xiàn)精確的細(xì)胞毒性作用。然而,諸如脫靶毒性、耐藥性和免疫相關(guān)不良事件等局限性仍需仔細(xì)評(píng)估和進(jìn)一步優(yōu)化。有必要開展進(jìn)一步研究,以探索BsAbs與其他抗腫瘤策略聯(lián)用的潛力,平衡療效與安全性,并優(yōu)化基于門診的給藥流程。通過(guò)追蹤近期獲批的BsAbs及處于臨床試驗(yàn)階段的BsAb候選藥物的研究進(jìn)展,可以明顯看出,BsAb作為一種新穎且具有變革性的選擇,在改善患者生存結(jié)局方面擁有巨大前景。
雙特異性抗體的分類與作用機(jī)制
雙特異性抗體(BsAbs)通過(guò)同時(shí)結(jié)合兩個(gè)不同靶點(diǎn),展現(xiàn)出超越單克隆抗體的協(xié)同效應(yīng)。從結(jié)構(gòu)上可分為含F(xiàn)c域的IgG樣BsAbs(如cadonilimab)和不含F(xiàn)c域的非IgG樣片段(如BiTE)。作用機(jī)制上,橋接型BsAbs(如blinatumomab)通過(guò)連接T細(xì)胞與腫瘤細(xì)胞觸發(fā)殺傷;抗原交聯(lián)型(如amivantamab)阻斷雙信號(hào)通路克服耐藥;輔因子模擬型(如emicizumab)則替代缺失蛋白功能。

圖1 雙特異性抗體開啟腫瘤治療新時(shí)代
血液腫瘤治療突破
在急性B淋巴細(xì)胞白血病(BCP-ALL)中,CD19×CD3雙抗blinatumomab使復(fù)發(fā)/難治患者中位生存期從4個(gè)月提升至7.7個(gè)月。針對(duì)多發(fā)性骨髓瘤(MM),BCMA×CD3雙抗teclistamab和GPRC5D×CD3雙抗talquetamab在四線治療中仍能實(shí)現(xiàn)60%以上的客觀緩解率(ORR)。值得注意的是,glofitamab采用2:1雙價(jià)CD20結(jié)合設(shè)計(jì),使彌漫大B細(xì)胞淋巴瘤(DLBCL)患者完全緩解(CR)率達(dá)39.4%。
實(shí)體瘤應(yīng)用進(jìn)展
非小細(xì)胞肺癌(NSCLC)領(lǐng)域,EGFR×c-MET雙抗amivantamab對(duì)EGFR 20號(hào)外顯子插入突變患者的中位無(wú)進(jìn)展生存期(mPFS)達(dá)11.4個(gè)月。宮頸癌(CC)治療中,PD-1×CTLA-4四價(jià)雙抗cadonilimab聯(lián)合化療使ORR提升至66.7%。此外,DLL3×CD3雙抗tarlatamab為小細(xì)胞肺癌(SCLC)后線治療帶來(lái)40%的ORR。
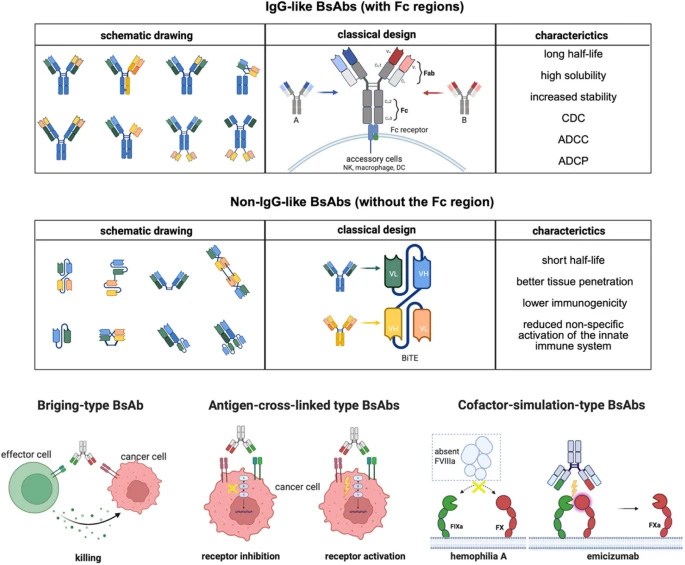
圖2 雙特異性抗體的分類與作用機(jī)制
挑戰(zhàn)與優(yōu)化策略
盡管療效顯著,BsAbs面臨CRS(發(fā)生率14-35%)、神經(jīng)毒性(ICANS)和靶向脫瘤效應(yīng)等挑戰(zhàn)。通過(guò)階梯給藥(如teclistamab)、皮下注射(如epcoritamab)及Fc工程化改造(如alnuctamab)可降低毒性。針對(duì)耐藥問(wèn)題,聯(lián)合PD-1抑制劑或CAR-T細(xì)胞治療(如CD19 CAR-T序貫blinatumomab)展現(xiàn)出協(xié)同潛力。
未來(lái)發(fā)展方向
當(dāng)前80%的BsAbs仍處于早期臨床階段,phase III候選藥物如PD-L1×TGF-β雙抗SHR-1701和HER2×HER3雙抗KN026值得關(guān)注。隨著給藥方案優(yōu)化(如talquetamab每月給藥)和門診管理模式推廣,BsAbs有望從"救援治療"進(jìn)階為"全程治療"支柱。
參考資料
[1] Bispecific antibodies: unleashing a new era in oncology treatment
摘要: 本綜述深入探討了免疫代謝在腫瘤微環(huán)境(TME)中的關(guān)鍵作用。
診斷與治療標(biāo)準(zhǔn)的進(jìn)步顯著提高了惡性腫瘤患者的生存率。然而,尋找有效策略以應(yīng)對(duì)耐藥性或復(fù)發(fā)性晚期腫瘤,仍然是一個(gè)至關(guān)重要且堅(jiān)定不移的目標(biāo)。雙特異性抗體(BsAbs)通過(guò)同時(shí)結(jié)合兩個(gè)不同靶點(diǎn),從而提高了特異性、最大程度減少了脫靶毒性,并能協(xié)同調(diào)節(jié)抗腫瘤免疫和腫瘤微環(huán)境,由此開啟了抗腫瘤治療的新時(shí)代。與兩種單克隆抗體聯(lián)用相比,BsAbs代表了雙特異性的物理整合,展現(xiàn)出更優(yōu)的結(jié)合效力,降低了耐藥風(fēng)險(xiǎn),并實(shí)現(xiàn)了獨(dú)特的生物學(xué)功能,例如橋接腫瘤細(xì)胞和T細(xì)胞以實(shí)現(xiàn)精確的細(xì)胞毒性作用。然而,諸如脫靶毒性、耐藥性和免疫相關(guān)不良事件等局限性仍需仔細(xì)評(píng)估和進(jìn)一步優(yōu)化。有必要開展進(jìn)一步研究,以探索BsAbs與其他抗腫瘤策略聯(lián)用的潛力,平衡療效與安全性,并優(yōu)化基于門診的給藥流程。通過(guò)追蹤近期獲批的BsAbs及處于臨床試驗(yàn)階段的BsAb候選藥物的研究進(jìn)展,可以明顯看出,BsAb作為一種新穎且具有變革性的選擇,在改善患者生存結(jié)局方面擁有巨大前景。
雙特異性抗體的分類與作用機(jī)制
雙特異性抗體(BsAbs)通過(guò)同時(shí)結(jié)合兩個(gè)不同靶點(diǎn),展現(xiàn)出超越單克隆抗體的協(xié)同效應(yīng)。從結(jié)構(gòu)上可分為含F(xiàn)c域的IgG樣BsAbs(如cadonilimab)和不含F(xiàn)c域的非IgG樣片段(如BiTE)。作用機(jī)制上,橋接型BsAbs(如blinatumomab)通過(guò)連接T細(xì)胞與腫瘤細(xì)胞觸發(fā)殺傷;抗原交聯(lián)型(如amivantamab)阻斷雙信號(hào)通路克服耐藥;輔因子模擬型(如emicizumab)則替代缺失蛋白功能。

圖1 雙特異性抗體開啟腫瘤治療新時(shí)代
血液腫瘤治療突破
在急性B淋巴細(xì)胞白血?。˙CP-ALL)中,CD19×CD3雙抗blinatumomab使復(fù)發(fā)/難治患者中位生存期從4個(gè)月提升至7.7個(gè)月。針對(duì)多發(fā)性骨髓瘤(MM),BCMA×CD3雙抗teclistamab和GPRC5D×CD3雙抗talquetamab在四線治療中仍能實(shí)現(xiàn)60%以上的客觀緩解率(ORR)。值得注意的是,glofitamab采用2:1雙價(jià)CD20結(jié)合設(shè)計(jì),使彌漫大B細(xì)胞淋巴瘤(DLBCL)患者完全緩解(CR)率達(dá)39.4%。
實(shí)體瘤應(yīng)用進(jìn)展
非小細(xì)胞肺癌(NSCLC)領(lǐng)域,EGFR×c-MET雙抗amivantamab對(duì)EGFR 20號(hào)外顯子插入突變患者的中位無(wú)進(jìn)展生存期(mPFS)達(dá)11.4個(gè)月。宮頸癌(CC)治療中,PD-1×CTLA-4四價(jià)雙抗cadonilimab聯(lián)合化療使ORR提升至66.7%。此外,DLL3×CD3雙抗tarlatamab為小細(xì)胞肺癌(SCLC)后線治療帶來(lái)40%的ORR。

圖2 雙特異性抗體的分類與作用機(jī)制
挑戰(zhàn)與優(yōu)化策略
盡管療效顯著,BsAbs面臨CRS(發(fā)生率14-35%)、神經(jīng)毒性(ICANS)和靶向脫瘤效應(yīng)等挑戰(zhàn)。通過(guò)階梯給藥(如teclistamab)、皮下注射(如epcoritamab)及Fc工程化改造(如alnuctamab)可降低毒性。針對(duì)耐藥問(wèn)題,聯(lián)合PD-1抑制劑或CAR-T細(xì)胞治療(如CD19 CAR-T序貫blinatumomab)展現(xiàn)出協(xié)同潛力。
未來(lái)發(fā)展方向
當(dāng)前80%的BsAbs仍處于早期臨床階段,phase III候選藥物如PD-L1×TGF-β雙抗SHR-1701和HER2×HER3雙抗KN026值得關(guān)注。隨著給藥方案優(yōu)化(如talquetamab每月給藥)和門診管理模式推廣,BsAbs有望從"救援治療"進(jìn)階為"全程治療"支柱。
參考資料
[1] Bispecific antibodies: unleashing a new era in oncology treatment



