摘要:研究人員近日開發(fā)出一種新方法,能夠從單個組織樣本中重建癌細胞的發(fā)育過程。
癌癥并非是一夜之間形成的?;蚪M中的促癌改變可能需要數(shù)十年的時間,才能最終導(dǎo)致惡性腫瘤的形成。
德國癌癥研究中心和英國牛津大學(xué)的研究人員近日開發(fā)出一種新方法,能夠從單個組織樣本中重建癌細胞的發(fā)育過程,也就是進化過程。這種進化研究尚處于起步階段。他們的愿望是利用新方法在早期階段檢測癌癥,最終目標(biāo)是阻斷這一過程。
這種名為SCIFER的新方法于7月3日發(fā)表在《Nature Genetics》雜志上。
生物體承受著自然選擇的壓力,意味著那些最能適應(yīng)環(huán)境的生物才能生存下來。這種自然選擇過程也發(fā)生在人體中。適應(yīng)力更強的細胞會擴散開來,其他細胞則被取代。
 圖1 體干細胞中克隆選擇的檢測與量化
圖1 體干細胞中克隆選擇的檢測與量化這種所謂的體細胞進化可能會對生物體產(chǎn)生積極的影響。然而,癌細胞特別強勢,它們會不受抑制地增殖,并在此過程中取代健康組織。
研究團隊的目標(biāo)是了解癌細胞的進化?!拔覀兊脑竿情_發(fā)一種新型的早期癌癥檢測方法。從最初的突變事件到肉眼可見的腫瘤,可能需要數(shù)十年時間。這也意味著,在很長一段時間內(nèi),我們有可能干預(yù)并阻止癌癥的發(fā)展。”
雖然距離這一目標(biāo)的實現(xiàn)還有很長的路要走,但研究人員通過他們開發(fā)的SCIFER方法邁出了第一步。
他們成功重建了人體細胞克?。磥碓从趩蝹€細胞的細胞簇)的進化過程。SCIFER方法能夠在早期階段檢測到快速生長的克隆。他們新開發(fā)的方法是以突變?yōu)榛A(chǔ)。隨著時間的推移,單個細胞中積累了數(shù)百個突變,由此產(chǎn)生的突變模式為研究團隊解讀細胞進化提供了線索。
共同通訊作者、德國癌癥研究中心的Thomas H?fer表示:“這些突變絕大多數(shù)是中性的,既不有利于細胞,也不有害于細胞。然而,如果發(fā)生一個致癌突變,讓細胞更加適應(yīng)環(huán)境,這將會改變許多中性突變的進化模式?!?/div> 圖1 體干細胞中克隆選擇的檢測與量化
圖1 體干細胞中克隆選擇的檢測與量化
“通過這種易于測定的變化,我們可以追溯致癌突變何時發(fā)生,以及相應(yīng)的癌前細胞克隆生長速度有多快。我們可以通過單個血液或組織樣本來計算時間線?!?/div>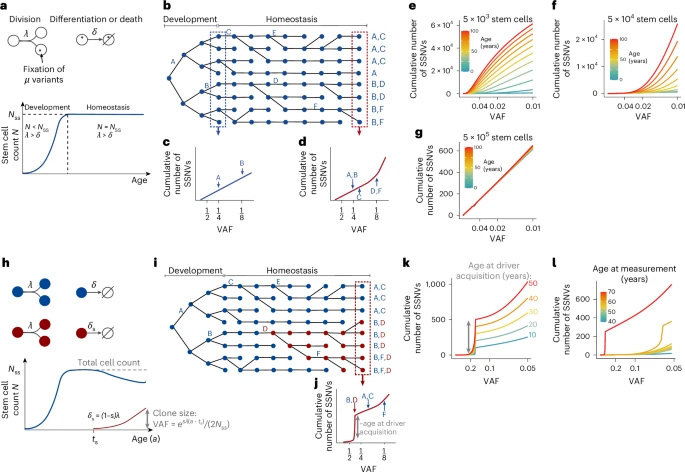
圖2 穩(wěn)態(tài)組織中漂變與選擇的群體遺傳學(xué)模型
此外,牛津大學(xué)血液學(xué)家Paresh Vyas及其團隊也參與了SCIFER的開發(fā)。他們提供了健康志愿者的寶貴骨髓樣本,以便全面測試該方法并使其適應(yīng)真實世界的數(shù)據(jù)。
通常來說,致癌基因處于關(guān)閉狀態(tài),或偶爾短暫激活。然而,突變的出現(xiàn)會導(dǎo)致致癌基因一直處于激活狀態(tài),從而增加癌癥發(fā)生的風(fēng)險。

圖2 穩(wěn)態(tài)組織中漂變與選擇的群體遺傳學(xué)模型
包括本研究在內(nèi)的一些研究已經(jīng)表明,致癌基因的突變發(fā)生頻率遠高于此前預(yù)期。然而,致癌基因的持續(xù)激活并不一定會導(dǎo)致癌癥。
“例如,我們發(fā)現(xiàn),大腦中攜帶突變致癌基因的細胞增殖速度更快,但并未發(fā)展成惡性腫瘤,”第一作者Verena K?rber報告稱。顯然,人體具備有效的保護機制,能夠抑制可能存在風(fēng)險的細胞。
單個激活的致癌基因通常不會導(dǎo)致癌癥。在大多數(shù)情況下,必須同時發(fā)生多個致癌突變,而非遺傳因素也可能發(fā)揮作用。例如,目前已知細胞微環(huán)境中的炎癥會增加惡性轉(zhuǎn)化的風(fēng)險。
在后續(xù)的研究中,研究人員希望弄清楚哪些選擇因素會促使致癌基因被激活的細胞進一步發(fā)生惡性轉(zhuǎn)化,以及哪些因素能夠阻止這一過程。他們的目標(biāo)是利用這一機制開發(fā)新的干預(yù)策略。
以骨髓增生異常綜合征 (MDS) 為例,這是一種造血干細胞疾病,可能發(fā)展成急性髓系白血病。然而,并非所有的MDS患者都會發(fā)展成白血病,因此,準確識別高危人群并提供有針對性的干預(yù)措施具有重大意義。
Thomas H?fer認為,以SCIFER為基礎(chǔ)的各類血癌的細胞進化研究,有望在未來取得具有臨床應(yīng)用價值的成果。
參考資料
[1] Detecting and quantifying clonal selection in somatic stem cells
摘要:研究人員近日開發(fā)出一種新方法,能夠從單個組織樣本中重建癌細胞的發(fā)育過程。
癌癥并非是一夜之間形成的?;蚪M中的促癌改變可能需要數(shù)十年的時間,才能最終導(dǎo)致惡性腫瘤的形成。
德國癌癥研究中心和英國牛津大學(xué)的研究人員近日開發(fā)出一種新方法,能夠從單個組織樣本中重建癌細胞的發(fā)育過程,也就是進化過程。這種進化研究尚處于起步階段。他們的愿望是利用新方法在早期階段檢測癌癥,最終目標(biāo)是阻斷這一過程。
這種名為SCIFER的新方法于7月3日發(fā)表在《Nature Genetics》雜志上。
生物體承受著自然選擇的壓力,意味著那些最能適應(yīng)環(huán)境的生物才能生存下來。這種自然選擇過程也發(fā)生在人體中。適應(yīng)力更強的細胞會擴散開來,其他細胞則被取代。
 圖1 體干細胞中克隆選擇的檢測與量化
圖1 體干細胞中克隆選擇的檢測與量化這種所謂的體細胞進化可能會對生物體產(chǎn)生積極的影響。然而,癌細胞特別強勢,它們會不受抑制地增殖,并在此過程中取代健康組織。
研究團隊的目標(biāo)是了解癌細胞的進化?!拔覀兊脑竿情_發(fā)一種新型的早期癌癥檢測方法。從最初的突變事件到肉眼可見的腫瘤,可能需要數(shù)十年時間。這也意味著,在很長一段時間內(nèi),我們有可能干預(yù)并阻止癌癥的發(fā)展?!?/div>
雖然距離這一目標(biāo)的實現(xiàn)還有很長的路要走,但研究人員通過他們開發(fā)的SCIFER方法邁出了第一步。
他們成功重建了人體細胞克?。磥碓从趩蝹€細胞的細胞簇)的進化過程。SCIFER方法能夠在早期階段檢測到快速生長的克隆。他們新開發(fā)的方法是以突變?yōu)榛A(chǔ)。隨著時間的推移,單個細胞中積累了數(shù)百個突變,由此產(chǎn)生的突變模式為研究團隊解讀細胞進化提供了線索。
共同通訊作者、德國癌癥研究中心的Thomas H?fer表示:“這些突變絕大多數(shù)是中性的,既不有利于細胞,也不有害于細胞。然而,如果發(fā)生一個致癌突變,讓細胞更加適應(yīng)環(huán)境,這將會改變許多中性突變的進化模式?!?/div>
“通過這種易于測定的變化,我們可以追溯致癌突變何時發(fā)生,以及相應(yīng)的癌前細胞克隆生長速度有多快。我們可以通過單個血液或組織樣本來計算時間線?!?/div>
圖2 穩(wěn)態(tài)組織中漂變與選擇的群體遺傳學(xué)模型
此外,牛津大學(xué)血液學(xué)家Paresh Vyas及其團隊也參與了SCIFER的開發(fā)。他們提供了健康志愿者的寶貴骨髓樣本,以便全面測試該方法并使其適應(yīng)真實世界的數(shù)據(jù)。
通常來說,致癌基因處于關(guān)閉狀態(tài),或偶爾短暫激活。然而,突變的出現(xiàn)會導(dǎo)致致癌基因一直處于激活狀態(tài),從而增加癌癥發(fā)生的風(fēng)險。

圖2 穩(wěn)態(tài)組織中漂變與選擇的群體遺傳學(xué)模型
包括本研究在內(nèi)的一些研究已經(jīng)表明,致癌基因的突變發(fā)生頻率遠高于此前預(yù)期。然而,致癌基因的持續(xù)激活并不一定會導(dǎo)致癌癥。
“例如,我們發(fā)現(xiàn),大腦中攜帶突變致癌基因的細胞增殖速度更快,但并未發(fā)展成惡性腫瘤,”第一作者Verena K?rber報告稱。顯然,人體具備有效的保護機制,能夠抑制可能存在風(fēng)險的細胞。
單個激活的致癌基因通常不會導(dǎo)致癌癥。在大多數(shù)情況下,必須同時發(fā)生多個致癌突變,而非遺傳因素也可能發(fā)揮作用。例如,目前已知細胞微環(huán)境中的炎癥會增加惡性轉(zhuǎn)化的風(fēng)險。
在后續(xù)的研究中,研究人員希望弄清楚哪些選擇因素會促使致癌基因被激活的細胞進一步發(fā)生惡性轉(zhuǎn)化,以及哪些因素能夠阻止這一過程。他們的目標(biāo)是利用這一機制開發(fā)新的干預(yù)策略。
以骨髓增生異常綜合征 (MDS) 為例,這是一種造血干細胞疾病,可能發(fā)展成急性髓系白血病。然而,并非所有的MDS患者都會發(fā)展成白血病,因此,準確識別高危人群并提供有針對性的干預(yù)措施具有重大意義。
Thomas H?fer認為,以SCIFER為基礎(chǔ)的各類血癌的細胞進化研究,有望在未來取得具有臨床應(yīng)用價值的成果。
參考資料
[1] Detecting and quantifying clonal selection in somatic stem cells



