摘要:軟腦膜轉(zhuǎn)移(LM)是實體瘤致命并發(fā)癥,雖有炎癥浸潤卻無法控制腫瘤。本研究通過小鼠模型和臨床樣本,發(fā)現(xiàn) IFNγ 由 T 細(xì)胞產(chǎn)生
軟腦膜(Leptomeninges)是包裹中樞神經(jīng)系統(tǒng)的腦脊液相隙,當(dāng)癌細(xì)胞侵入形成軟腦膜轉(zhuǎn)移(LM)時,會引發(fā)類似腦膜炎的強烈炎癥反應(yīng),卻詭異般地允許腫瘤細(xì)胞存活甚至增殖。這種 “無效炎癥” 現(xiàn)象長期困擾學(xué)界:為何豐富的免疫細(xì)胞浸潤未能遏制腫瘤?傳統(tǒng)觀點認(rèn)為,中樞神經(jīng)系統(tǒng)的免疫特權(quán)可能削弱了抗腫瘤應(yīng)答,但 LM 卻展現(xiàn)出獨特的炎癥特征,尤其是干擾素 -γ(IFNγ)的異常表達(dá)。既往研究發(fā)現(xiàn),LM 患者腦脊液中 IFNγ 水平升高與免疫細(xì)胞募集相關(guān),但 IFNγ 在 LM 微環(huán)境中究竟扮演促癌還是抑癌角色,其作用機制如何,仍是未解之謎。
為破解這一難題,紀(jì)念斯隆凱特琳癌癥中心(Memorial Sloan Kettering Cancer Center)的研究團(tuán)隊展開了深入探索。他們結(jié)合臨床樣本多組學(xué)分析與免疫健全小鼠模型,系統(tǒng)解析了軟腦膜微環(huán)境中免疫細(xì)胞與腫瘤細(xì)胞的互作網(wǎng)絡(luò),最終在《Nature》發(fā)表研究成果,揭示了 IFNγ 調(diào)控軟腦膜抗腫瘤免疫的獨特機制。
 圖1 干擾素-γ協(xié)調(diào)軟腦膜抗腫瘤應(yīng)答
圖1 干擾素-γ協(xié)調(diào)軟腦膜抗腫瘤應(yīng)答研究采用的關(guān)鍵技術(shù)包括:①臨床樣本分析:收集乳腺癌、肺癌等患者的腦脊液(CSF),通過單細(xì)胞轉(zhuǎn)錄組測序(scRNA-seq)和靶向蛋白質(zhì)組學(xué)( proximity extension assay)分析免疫細(xì)胞組成和細(xì)胞因子譜;②動物模型構(gòu)建:利用同基因小鼠建立肺癌、乳腺癌、黑色素瘤的 LM 模型(LeptoM),通過基因敲除(如 Ifng-/-、Ifngr1-/-)和病毒載體(AAV)介導(dǎo)的基因過表達(dá),解析 IFNγ 的功能;③免疫細(xì)胞示蹤與功能驗證:結(jié)合流式細(xì)胞術(shù)、細(xì)胞命運軌跡分析(CellRank、Palantir)和骨髓嵌合技術(shù),追蹤樹突狀細(xì)胞(DC)和自然殺傷細(xì)胞(NK)的分化與激活路徑。
軟腦膜轉(zhuǎn)移的炎癥特征與 IFNγ 的核心作用
通過分析 LM 患者腦脊液,研究發(fā)現(xiàn)其呈現(xiàn)顯著的炎癥性細(xì)胞增多(pleocytosis),包含 T 細(xì)胞、NK 細(xì)胞、單核巨噬細(xì)胞及 DC 等,其中 IFNγ 是乳腺癌、肺癌、黑色素瘤等多種腫瘤來源 LM 患者腦脊液中共同上調(diào)的細(xì)胞因子。臨床數(shù)據(jù)顯示,IFNγ 水平升高與患者總生存期延長相關(guān),提示其抗腫瘤作用。在免疫健全小鼠模型中,敲除 Ifng 或其受體 Ifngr1 均導(dǎo)致軟腦膜腫瘤失控生長,而過表達(dá) IFNγ 則顯著抑制腫瘤,證實 IFNγ 是軟腦膜抗腫瘤應(yīng)答的核心調(diào)控因子。
IFNγ 的來源與作用靶點:T 細(xì)胞→DC 的信號軸
進(jìn)一步研究發(fā)現(xiàn),軟腦膜中的 IFNγ 主要由 T 細(xì)胞產(chǎn)生,NK 細(xì)胞貢獻(xiàn)較小。IFNγ 通過結(jié)合 DC 表面受體,激活 STAT1 信號通路,促進(jìn)常規(guī) DC(cDC)尤其是 cDC2 亞群成熟為遷移性 CCR7+ DC。軌跡分析顯示,cDC2 向 CCR7+ DC 的分化依賴 IFNγ,且這一過程不依賴抗原呈遞。通過骨髓嵌合實驗和特異性細(xì)胞耗竭技術(shù),證實 cDC 的完整性是 IFNγ 發(fā)揮抗腫瘤作用的必要條件,而巨噬細(xì)胞和中性粒細(xì)胞則非必需。
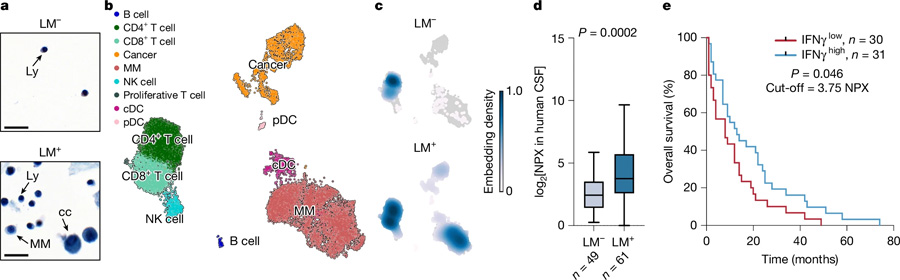
圖2 炎癥誘導(dǎo)的腦脊液細(xì)胞增多見于軟腦膜轉(zhuǎn)移患者
CCR7+ DC 與 NK 細(xì)胞的協(xié)同抗腫瘤機制
CCR7+ DC 通過分泌 IL-12 和 IL-15 等細(xì)胞因子,激活 NK 細(xì)胞的增殖與細(xì)胞毒性。在 LM 微環(huán)境中,NK 細(xì)胞表現(xiàn)為活化和增殖表型,其殺傷功能依賴 CCR7+ DC 的信號支持。阻斷 NK 細(xì)胞或敲除其受體基因,均導(dǎo)致 IFNγ 的抗腫瘤效應(yīng)喪失。機制上,IFNγ 通過 “T 細(xì)胞 - CCR7+ DC-NK 細(xì)胞” 軸,形成非抗原依賴的固有免疫抗腫瘤環(huán)路,誘導(dǎo)腫瘤細(xì)胞凋亡(如 cleaved caspase-3 表達(dá)升高)。
軟腦膜特異性免疫機制的啟示
與其他組織不同,軟腦膜中的 IFNγ 效應(yīng)不依賴 MHC 分子介導(dǎo)的適應(yīng)性免疫,而是通過固有免疫細(xì)胞互作實現(xiàn)。這解釋了為何靶向適應(yīng)性免疫的臨床療法(如 PD-1 抑制劑)在 LM 中療效有限。研究還發(fā)現(xiàn),軟腦膜 DC 主要來源于外周骨髓,而非局部中樞神經(jīng)系統(tǒng),其遷移和分化受 IFNγ 調(diào)控,提示通過局部遞送 IFNγ 或激活 DC-NK 軸可能是更有效的治療策略。
研究意義與未來方向
該研究首次系統(tǒng)闡釋了軟腦膜微環(huán)境中 IFNγ 的雙重角色:其不僅是炎癥標(biāo)志物,更是驅(qū)動固有免疫抗腫瘤的關(guān)鍵因子,揭示了 “T 細(xì)胞 - DC-NK 細(xì)胞” 軸在軟腦膜中的獨特作用。這一發(fā)現(xiàn)突破了傳統(tǒng)認(rèn)知,為 LM 治療提供了新靶點 —— 通過激活 CCR7+ DC 或增強 NK 細(xì)胞功能,有望開發(fā)針對中樞神經(jīng)系統(tǒng)轉(zhuǎn)移的新型免疫療法。此外,研究建立的 LM 小鼠模型和多組學(xué)分析方法,為解析其他中樞神經(jīng)系統(tǒng)腫瘤的免疫機制提供了重要工具。未來研究可進(jìn)一步探索 IFNγ 與其他免疫檢查點的聯(lián)合應(yīng)用,或開發(fā)靶向軟腦膜的藥物遞送系統(tǒng),以提升治療精準(zhǔn)性。
參考資料
[1] Interferon-γ orchestrates leptomeningeal anti-tumour response
摘要:軟腦膜轉(zhuǎn)移(LM)是實體瘤致命并發(fā)癥,雖有炎癥浸潤卻無法控制腫瘤。本研究通過小鼠模型和臨床樣本,發(fā)現(xiàn) IFNγ 由 T 細(xì)胞產(chǎn)生
軟腦膜(Leptomeninges)是包裹中樞神經(jīng)系統(tǒng)的腦脊液相隙,當(dāng)癌細(xì)胞侵入形成軟腦膜轉(zhuǎn)移(LM)時,會引發(fā)類似腦膜炎的強烈炎癥反應(yīng),卻詭異般地允許腫瘤細(xì)胞存活甚至增殖。這種 “無效炎癥” 現(xiàn)象長期困擾學(xué)界:為何豐富的免疫細(xì)胞浸潤未能遏制腫瘤?傳統(tǒng)觀點認(rèn)為,中樞神經(jīng)系統(tǒng)的免疫特權(quán)可能削弱了抗腫瘤應(yīng)答,但 LM 卻展現(xiàn)出獨特的炎癥特征,尤其是干擾素 -γ(IFNγ)的異常表達(dá)。既往研究發(fā)現(xiàn),LM 患者腦脊液中 IFNγ 水平升高與免疫細(xì)胞募集相關(guān),但 IFNγ 在 LM 微環(huán)境中究竟扮演促癌還是抑癌角色,其作用機制如何,仍是未解之謎。
為破解這一難題,紀(jì)念斯隆凱特琳癌癥中心(Memorial Sloan Kettering Cancer Center)的研究團(tuán)隊展開了深入探索。他們結(jié)合臨床樣本多組學(xué)分析與免疫健全小鼠模型,系統(tǒng)解析了軟腦膜微環(huán)境中免疫細(xì)胞與腫瘤細(xì)胞的互作網(wǎng)絡(luò),最終在《Nature》發(fā)表研究成果,揭示了 IFNγ 調(diào)控軟腦膜抗腫瘤免疫的獨特機制。
 圖1 干擾素-γ協(xié)調(diào)軟腦膜抗腫瘤應(yīng)答
圖1 干擾素-γ協(xié)調(diào)軟腦膜抗腫瘤應(yīng)答研究采用的關(guān)鍵技術(shù)包括:①臨床樣本分析:收集乳腺癌、肺癌等患者的腦脊液(CSF),通過單細(xì)胞轉(zhuǎn)錄組測序(scRNA-seq)和靶向蛋白質(zhì)組學(xué)( proximity extension assay)分析免疫細(xì)胞組成和細(xì)胞因子譜;②動物模型構(gòu)建:利用同基因小鼠建立肺癌、乳腺癌、黑色素瘤的 LM 模型(LeptoM),通過基因敲除(如 Ifng-/-、Ifngr1-/-)和病毒載體(AAV)介導(dǎo)的基因過表達(dá),解析 IFNγ 的功能;③免疫細(xì)胞示蹤與功能驗證:結(jié)合流式細(xì)胞術(shù)、細(xì)胞命運軌跡分析(CellRank、Palantir)和骨髓嵌合技術(shù),追蹤樹突狀細(xì)胞(DC)和自然殺傷細(xì)胞(NK)的分化與激活路徑。
軟腦膜轉(zhuǎn)移的炎癥特征與 IFNγ 的核心作用
通過分析 LM 患者腦脊液,研究發(fā)現(xiàn)其呈現(xiàn)顯著的炎癥性細(xì)胞增多(pleocytosis),包含 T 細(xì)胞、NK 細(xì)胞、單核巨噬細(xì)胞及 DC 等,其中 IFNγ 是乳腺癌、肺癌、黑色素瘤等多種腫瘤來源 LM 患者腦脊液中共同上調(diào)的細(xì)胞因子。臨床數(shù)據(jù)顯示,IFNγ 水平升高與患者總生存期延長相關(guān),提示其抗腫瘤作用。在免疫健全小鼠模型中,敲除 Ifng 或其受體 Ifngr1 均導(dǎo)致軟腦膜腫瘤失控生長,而過表達(dá) IFNγ 則顯著抑制腫瘤,證實 IFNγ 是軟腦膜抗腫瘤應(yīng)答的核心調(diào)控因子。
IFNγ 的來源與作用靶點:T 細(xì)胞→DC 的信號軸
進(jìn)一步研究發(fā)現(xiàn),軟腦膜中的 IFNγ 主要由 T 細(xì)胞產(chǎn)生,NK 細(xì)胞貢獻(xiàn)較小。IFNγ 通過結(jié)合 DC 表面受體,激活 STAT1 信號通路,促進(jìn)常規(guī) DC(cDC)尤其是 cDC2 亞群成熟為遷移性 CCR7+ DC。軌跡分析顯示,cDC2 向 CCR7+ DC 的分化依賴 IFNγ,且這一過程不依賴抗原呈遞。通過骨髓嵌合實驗和特異性細(xì)胞耗竭技術(shù),證實 cDC 的完整性是 IFNγ 發(fā)揮抗腫瘤作用的必要條件,而巨噬細(xì)胞和中性粒細(xì)胞則非必需。

圖2 炎癥誘導(dǎo)的腦脊液細(xì)胞增多見于軟腦膜轉(zhuǎn)移患者
CCR7+ DC 與 NK 細(xì)胞的協(xié)同抗腫瘤機制
CCR7+ DC 通過分泌 IL-12 和 IL-15 等細(xì)胞因子,激活 NK 細(xì)胞的增殖與細(xì)胞毒性。在 LM 微環(huán)境中,NK 細(xì)胞表現(xiàn)為活化和增殖表型,其殺傷功能依賴 CCR7+ DC 的信號支持。阻斷 NK 細(xì)胞或敲除其受體基因,均導(dǎo)致 IFNγ 的抗腫瘤效應(yīng)喪失。機制上,IFNγ 通過 “T 細(xì)胞 - CCR7+ DC-NK 細(xì)胞” 軸,形成非抗原依賴的固有免疫抗腫瘤環(huán)路,誘導(dǎo)腫瘤細(xì)胞凋亡(如 cleaved caspase-3 表達(dá)升高)。
軟腦膜特異性免疫機制的啟示
與其他組織不同,軟腦膜中的 IFNγ 效應(yīng)不依賴 MHC 分子介導(dǎo)的適應(yīng)性免疫,而是通過固有免疫細(xì)胞互作實現(xiàn)。這解釋了為何靶向適應(yīng)性免疫的臨床療法(如 PD-1 抑制劑)在 LM 中療效有限。研究還發(fā)現(xiàn),軟腦膜 DC 主要來源于外周骨髓,而非局部中樞神經(jīng)系統(tǒng),其遷移和分化受 IFNγ 調(diào)控,提示通過局部遞送 IFNγ 或激活 DC-NK 軸可能是更有效的治療策略。
研究意義與未來方向
該研究首次系統(tǒng)闡釋了軟腦膜微環(huán)境中 IFNγ 的雙重角色:其不僅是炎癥標(biāo)志物,更是驅(qū)動固有免疫抗腫瘤的關(guān)鍵因子,揭示了 “T 細(xì)胞 - DC-NK 細(xì)胞” 軸在軟腦膜中的獨特作用。這一發(fā)現(xiàn)突破了傳統(tǒng)認(rèn)知,為 LM 治療提供了新靶點 —— 通過激活 CCR7+ DC 或增強 NK 細(xì)胞功能,有望開發(fā)針對中樞神經(jīng)系統(tǒng)轉(zhuǎn)移的新型免疫療法。此外,研究建立的 LM 小鼠模型和多組學(xué)分析方法,為解析其他中樞神經(jīng)系統(tǒng)腫瘤的免疫機制提供了重要工具。未來研究可進(jìn)一步探索 IFNγ 與其他免疫檢查點的聯(lián)合應(yīng)用,或開發(fā)靶向軟腦膜的藥物遞送系統(tǒng),以提升治療精準(zhǔn)性。
參考資料
[1] Interferon-γ orchestrates leptomeningeal anti-tumour response



